Savasav-képlet, tulajdonságok, kockázatok és felhasználások
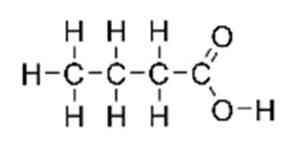
az vajsav, n-butánsav néven is ismert (az IUPAC rendszerben) a CH3CH2CH2-COOH szerkezeti képlettel rendelkező karbonsav. Rövid láncú zsírsavnak minősül. Kellemetlen szaga, csípős íze és egyidejűleg egy kicsit édes (az éterhez hasonló), szerkezete az 1. ábrán látható..
Elsősorban rancid vajban, parmezán sajtban, nyers tejben, állati zsírokban, növényi olajokban és hányásban találhatók. A neve a görög βουτυρος szóból származik, vagyis a „vaj” (közreműködők, 2016).
A vajsavat az emberi vastagbélben szénhidrátok bakteriális fermentációjával (beleértve az étrendi rostot is) képződik, és feltételezhetően elnyomja a vastagbélrákot..
A vajsav egy zsírsav formájában észterek az állati zsírok és növényi olajok. Érdekes, kis molekulatömegű a butánsav észterei, mint például a butirát, van aromák vagy ízesítőanyagok többnyire kellemes (a metabolomikus inovation központ, S. F.).
index
- 1 A vajsav fizikai és kémiai tulajdonságai
- 2 Reaktivitás és veszélyek
- 3 Alkalmazások és előnyök az egészségre
- 4 Referenciák
A vajsav fizikai és kémiai tulajdonságai
A vajsav színtelen folyadék, melynek kellemetlen szaga a retekes vaj. Bizonyos ízű vajjal is rendelkezik.
A molekulatömege 88,11 g / mol, sűrűsége 0,9528 g / ml szobahőmérsékleten. Olvadáspontja -5,1 ° C, forráspontja 163,75 ° C.
A vegyület jól oldódik vízben, etanolban és éterben. Ez kis mértékben oldódik szén-tetrakloridban. Ez egy gyenge sav, ami azt jelenti, hogy nem teljesen disszociál, pKa 4.82 (National Center for Biotechnology Information, S. F.).
Izomer, 2-metil-propánsav (izobutir), (CH3) 2CHCO2H, mind szabad állapotban, mind etil-észterében néhány növényi olajban megtalálható. Bár kereskedelmi szempontból kevésbé fontos, mint a vajsav (Brown, 2011).
A vajsav oxidálószerekkel reagálhat. 100 ° C feletti króm-trioxiddal az izzási reakciók lépnek fel. Ezek sem kompatibilisek a bázisokkal és a redukálószerekkel. Megtámadhatja az alumíniumot és más könnyűfémeket (BUTYRIC ACID, 2016).
Reaktivitás és veszélyek
A vajsavat gyúlékony vegyületnek tekintjük. Nem összeférhető erős oxidálószerekkel, alumíniummal és a legtöbb más közönséges fémvel, lúgokkal, redukálószerekkel (Royal Society of Chemistry, 2015).
A vegyület nagyon veszélyes a bőrrel való érintkezés esetén (égési sérülést okozhat), lenyelés, szembe jutás (irritáló) és belégzés esetén (súlyos légúti irritációt okozhat).
A permetezőfolyadék vagy a köd szövetkárosodást okozhat, különösen a szem, a száj és a légutak nyálkahártyáiban.
Az anyag mérgező a tüdőbe, az idegrendszer, a nyálkahártyákat. Ismételt vagy hosszan tartó expozíció a képes kárt ezekben a szervekben és a légúti irritációt, ami gyakran a hörgők fertőzés (Material Safety Data Sheet Vajsav- 2013).
Szembe kerülés esetén ellenőrizni kell, hogy az áldozat kontaktlencsével rendelkezik-e, és távolítsa el őket. Az áldozat szemeit vízzel vagy normál sóoldattal 20-30 percig kell mosni, miközben kórházat hívnak.
A bőrrel való érintkezés esetén az érintett területet vízbe kell meríteni, miközben eltávolítja és szigeteli az összes szennyezett ruhát. Óvatosan mossa le a bőr minden érintett területét szappannal és vízzel. Orvosi figyelmet kell szerezni.
Belélegzés esetén a szennyezett területet hűvös helyre kell hagyni. Ha tünetek alakulnak ki (pl. Zihálás, köhögés, légszomj vagy a szájban, a torokban vagy a mellkasban égő), forduljon orvoshoz.
Lenyelés esetén a hányást nem szabad kiváltani. Ha a sérült eszméleténél van, és nem rángatózott, kell beadni 1 vagy 2 pohár vizet, hogy híg a kémiai és hívja a kórházat vagy a mérgezési.
Ha az áldozat görcsös vagy tudattalan, nem szabad semmit adni szájon, biztosítja, hogy a légutak nyitva van, és az áldozat helyezze az áldozat oldalán kisebb, mint a test fejét. Ha azonnal forduljon orvoshoz.
Alkalmazások és előnyök az egészségre
A vajsav alacsony molekulatömegű észterei, mint például a metil-butirát, szaga és íze, általában kellemes. Emiatt élelmiszer- és parfüm-adalékanyagként használják őket.
A butirát, a vajsav konjugált bázisa természetesen több élelmiszerben található. Kiegészítő vagy ízesítőszerként is adható.
A vajsav vagy a butirátok észterei a növényi olaj mesterséges ízeinek és esszenciáinak előállítására szolgálnak. A butil-amirát a sárgabarackolaj fő összetevője, míg a metil-butirát ananászolajban található.
Az ananászolajat ízesítőszerként használják a csontnövekedés előmozdítására, a fogászati műtétek kezelésére és a megfázás, a torokfájás és az akut sinusitis kezelésére, a természetes termékek OCA Brazil szerint (PULUGURTHA, 2015) szerint.
A gyomor-bélrendszerben található baktériumok jelentős mennyiségű fermentáló butirátot, diétás rostot és nem emészthető szénhidrátokat termelhetnek. A rostokban gazdag ételek, mint az árpa, zab, barna rizs és korpa fogyasztása egészséges módja annak, hogy butirátot kapj a szervezetedben.
A "Journal of Nutrition" 2010. novemberi számában megjelent tanulmány azt jelzi, hogy a gabonafélék éjszaka gazdag, nem emészthető szénhidrátokban gazdag étele másnap reggel növelheti a plazma butirát koncentrációját..
Hozzáteszi, hogy ez lehet az a mechanizmus, amellyel a teljes kiőrlés megelőzi a cukorbetegséget és a szívbetegségeket.
A vajsavat, mint a butirátot, az emberi vastagbélben alakítják ki a rost fermentáció termékének, és ezt javasoljuk olyan tényezőnek, amely megmagyarázza, miért védik a magas rosttartalmú étrend a vastagbélrák megelőzésében..
Ennek a kapcsolatnak a lehetséges mechanizmusára vonatkozóan számos hipotézist vizsgáltak, beleértve, hogy a butirát fontos-e az epiteliális sejtek normális fenotípusos expressziójának fenntartásához, vagy javítja a sérült sejtek eltávolítását apoptózis útján..
A vajsav vagy a butirát további előnyei:
- Segítség a fogyásban.
- Csökkenti az irritált vastagbél szindrómát (Andrzej Załęski, 2013).
- Crohn-betegség kezelése (Ax, S.F.).
- Az inzulinrezisztencia elleni küzdelem.
- Gyulladásgátló hatású.
referenciák
- Andrzej Załęski, A. B. (2013). Vajsav irritábilis bél szindrómában. Przegla̜d Gastroenterologiczny, 350-353. A ncbi.nlm.nih.gov.
- Ax, J. (S.F.). Mi a vajsav? 6 Tudnivalók a tejsav előnyökről. A draxe-ből: draxe.com.
- Brown, W. H. (2011, december 2.). Vajsav (CH3CH2CH2CO2H). A britannica enciklopédiából származik: A britannica.com-ból visszanyert.
- BUTYRIC-sav. (2016). Felvétel a kémiai anyagokból: cameochemicals.noaa.gov.
- közreműködők, N. W. (2016, december 22.). Vajsav. Az új világ enciklopédiájából szerezhető be: A (z) newworldencyclopedia.org webhelyről.
- Anyagbiztonsági adatlap A vajsav. (2013, május 21.). A sciencelab-ből származik: sciencelab.com.
- Nemzeti Biotechnológiai Információs Központ. (S. F.). PubChem összetett adatbázis; CID = 264. A PubChem-ből: ncbi.nlm.nih.gov.
- PULUGURTHA, S. (2015, június 1.). Milyen élelmiszerek vannak a butirátban? A livestrong-ból: livestrong.com.
- Királyi Kémiai Társaság. (2015). Butánsav. A chemspider-ből származik: chemspider.com.
- a metabolomikus innovációs központ. (S. F.). Emberi anyagcsere-adatbázis, amely a vajsav metabokartját mutatja. A (z) hmdb.ca webhelyről: hmdb.ca.


