Berillium-hidroxid (Be (OH) 2) kémiai szerkezete, tulajdonságai és felhasználása
az berillium-hidroxid egy kémiai vegyület, amely két hidroxid (OH) molekulából és egy berillium (Be) molekulából áll. Kémiai képlete Be (OH)2 és amfoter fajnak minősül. Általában a berillium-monoxid és a víz közötti reakcióból nyerhető, a következő kémiai reakció szerint: BeO + H2O → Be (OH)2
Másrészt, ez az amfoter anyag molekuláris konfigurációja lineáris. Azonban a berillium-hidroxid különböző szerkezetei: alfa- és béta-forma, ásványi anyagként és gőzfázisban, az alkalmazott módszertől függően..
index
- 1 Kémiai szerkezet
- 1.1. Beryllium-hidroxid alfa
- 1.2 Béta-berilium-hidroxid
- 1.3. Berillium-hidroxid ásványi anyagokban
- 1.4 A berillium-hidroxid gőze
- 2 Tulajdonságok
- 2.1 Megjelenés
- 2.2 Termokémiai tulajdonságok
- 2.3 Oldhatóság
- 2.4 Az expozícióból eredő kockázatok
- 3 Használat
- 4
- 4.1 Fémes berillium beszerzése
- 5 Referenciák
Kémiai szerkezet
Ez a kémiai vegyület négy különböző módon megtalálható:
Az alfa-berilium-hidroxid
Bármely bázikus reagens, például nátrium-hidroxid (NaOH) hozzáadásával a berillium-só oldatához a berillium-hidroxid alfa (α) formáját kapjuk. Az alábbi példa látható:
2NaOH (hígított) + BeCl2 → Be (OH)2↓ + 2NaCl
2NaOH (hígított) + BeSO4 → Be (OH)2↓ + Na2SW4
Beryllium-béta-hidroxid
Ennek az alfa-terméknek a degenerációja egy meta-stabil tetragonális kristályszerkezetet képez, amely hosszabb idő után rombos szerkezetű, beryllium-hidroxid béta (β) néven alakult át..
Ezt a béta formát is kapjuk csapadék formájában nátrium-berillium-oldatból hidrolízissel az olvadáspont közelében..
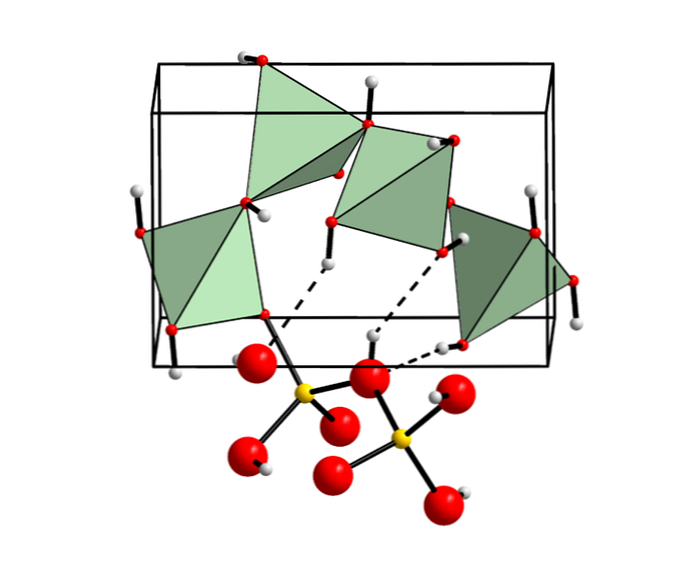
Berillium-hidroxid ásványi anyagokban
Habár nem szokásos, a berillium-hidroxid kristályos ásványi anyagként ismert, amit viselkedésnek neveznek (ilyen módon a kémiai összetételére hivatkozva)..
A Gadolinite (szilikátcsoport ásványai) átalakításával keletkező granitikus pegmatitokban vulkáni fumarolokban fordul elő..
Ez a viszonylag új ásványi anyagot először 1964-ben fedezték fel, és jelenleg csak az Egyesült Államokban, Texasban és Utahban található gránit pegmatitákban találták meg..
A berillium-hidroxid gőze
1200 ° C feletti hőmérsékleten (2190 ° C) a gőzfázisban a berillium-hidroxid létezik. A vízgőz és a berillium-oxid (BeO) közötti reakcióból nyerhető..
Hasonlóképpen, a kapott gőz részleges nyomása 73 Pa, 1500 ° C hőmérsékleten mérve.
tulajdonságok
A berillium-hidroxid móltömege vagy hozzávetőleges molekulatömege 43,0268 g / mol, sűrűsége 1,92 g / cm3.3. Olvadáspontja 1000 ° C-os hőmérsékleten van, amelyben a bomlása megkezdődik.
Ásványi anyagként a Be (OH)2 (behoita) keménysége 4 és sűrűsége 1,91 g / cm3 és 1,93 g / cm3.
megjelenés
A berillium-hidroxid fehér szilárd anyag, amely alfa-formában zselatin és amorf megjelenésű. Másrészt ennek a vegyületnek a béta formája egy jól meghatározott, orthorhombikus és stabil kristályszerkezetből áll..
Elmondható, hogy a Be (OH) ásványának morfológiája2 változatos, mert retikuláris kristályok, arborescent vagy gömb alakú aggregátumokként találhatók. Hasonlóképpen, fehér, rózsaszín, kékes, sőt színtelen és zsíros üveges fényű.
Termokémiai tulajdonságok
A képződés entalpiája: -902,5 kJ / mol
Gibbs-energia: -815,0 kJ / mol
A képződés entrópiája: 45,5 J / mol
Hőteljesítmény: 62,1 J / mol
Speciális hőteljesítmény: 1 443 J / K
A képződés standard entalpiája: -20,98 kJ / g
oldhatóság
A berillium-hidroxid amfoter jellegű, így képes protonokat adni vagy elfogadni, és savas és bázisos reakcióban oldja fel a savas és bázikus táptalajt, sót és vizet termel.
Ebben az értelemben a Be (OH) oldhatósága2 a vízben lévő oldatot a Kps oldhatósági termék korlátozza(H2O), ami 6,92 × 10-22.
Az expozíciós kockázatok
A legfeljebb 0,002 mg / m koncentrációban meghatározott berillium-hidroxid-anyag jogilag megengedett emberi expozíciós határértéke (PEL vagy OSHA).3 és 0,005 mg / m3 8 óra, és 0,0225 mg / m koncentráció esetén3 legfeljebb 30 perc.
Ezek a korlátozások abból adódnak, hogy a berilliumot az A1 típusú rákkeltő anyagnak (emberben a rákkeltő anyagnak a epidemiológiai vizsgálatokból származó bizonyítékok mennyisége alapján) osztályozzák..
alkalmazások
A berillium-hidroxid nyersanyagként való felhasználása bizonyos termékek feldolgozásához nagyon korlátozott (és szokatlan). Ez azonban olyan vegyület, amelyet fő reagensként használnak más vegyületek előállítására és berillium-fém előállítására.
megszerzése
A berillium-oxid (BeO) a nagy tisztaságú beryllium kémiai vegyülete, amelyet az iparban használnak. Színtelen szilárd anyagként jellemezhető, elektromos tulajdonságokkal és nagy hővezető képességgel.
Ebben az értelemben az elsődleges iparág szintézisének folyamatát (technikai minőségben) a következőképpen végzik:
- A berillium-hidroxidot kénsavban oldjuk (H2SW4).
- Amikor a reakciót végrehajtjuk, az oldatot szűrjük, így az oldhatatlan oxidok vagy szulfát szennyeződések kikerülnek..
- A szűrletet bepárlással bepároljuk, hogy a terméket koncentráljuk, amelyet lehűtünk, és így kapjuk a BeSO kristályokat.4.
- A BeSO4 a hőmérsékletet 1100 ° C és 1400 ° C közötti hőmérsékleten kalcináljuk.
A végterméket (BeO) ipari kerámia darabok gyártására használják.
Fémes berillium beszerzése
A berillium ásványi anyagok kitermelése és feldolgozása során szennyeződések keletkeznek, például a berillium-oxid és a berillium-hidroxid. Az utóbbit egy sor transzformációnak vetjük alá a fém berillium előállítása előtt.
A Be (OH) reagál2 ammónium-bifluorid oldattal:
Be (OH)2 + 2 (NH4) HF2 → (NH4)2BeF4 + 2 H2O
Az (NH4)2BeF4 hőmérséklet-növekedésnek van kitéve, termikus bomlással:
(NH4)2BeF4 → 2NH3 + 2HF + BeF2
Végül a berillium-fluorid redukciója 1300 ° C-on magnéziummal (Mg) beryllium-fémből áll:
BeF2 + Mg → Be + MgF2
A berilliumot fémötvözetekben, elektronikus alkatrészek gyártásában, röntgensugaras készülékek gyártásában használják..
referenciák
- Wikipedia. (N.d.). Berillium-hidroxid. A (z) en.wikipedia.org webhelyről származik
- Holleman, A. F .; Wiberg, E. és Wiberg, N. (2001). Berillium-hidroxid. A következőt kapta: books.google.co.ve
- Publishing, D. D. (s.f.). Behoite. A handbookofmineralogy.org-ról származik
- Minden reakció. (N.d.). Beryllium-hidroxid Be (OH)2. Az allreactions.com webhelyről származó
- Pubchem. (N.d.). Berillium-hidroxid. A pubchem.ncbi.nlm.nih.gov
- Walsh, K. A. és Vidal, E. E. (2009). Berillium-kémia és feldolgozás. A következőt kapta: books.google.co.ve


