Exoterm reakció, típusok és példák
az exoterm reakció egy olyan kémiai reakció típusa, amelyben energiaátvitel történik, főként hő vagy fénykibocsátás formájában. A név a görög előtagból származik exo, ami azt jelenti, hogy "külföldön"; és a "hő" kifejezés, amely hőre vagy hőmérsékletre utal.
Ebben az értelemben az exoterm reakciók más típusú energiákat vihetnek át a környezetbe, ahol keletkeznek, például robbanásokkal és a kinetikus és hangenergia átvitelének módjával, amikor a magas hőmérsékleten gázfázisú anyagok kibővülnek. erőszakos módon.
Ugyanígy az akkumulátorok használata esetén exoterm reakció is végbemegy, csak ebben az esetben szállítják az elektromos energiát..
index
- 1 Folyamat
- 2 típus
- 2.1 Égési reakciók
- 2.2 Semlegesítési reakciók
- 2.3 Oxidációs reakciók
- 2.4 Termit reakció
- 2.5 Reakciós polimerizáció
- 2.6 Nukleáris hasadási reakció
- 2.7 Egyéb reakciók
- 3 Példák
- 4 Referenciák
folyamat
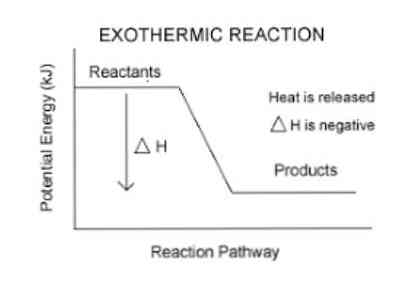
Korábban megemlítették, hogy egy exoterm reakció bekövetkezésekor energia-felszabadulás lép fel, amely könnyebben láthatóvá válik az alábbi egyenletben:
Reagensek → Termék (ek) + Energia
Tehát a rendszer által elnyelt vagy felszabaduló energia mennyiségi meghatározásához termodinamikai paramétert, az entalpiát ("H" néven jelöljük) használjuk. Ha egy rendszerben (ebben az esetben egy kémiai reakció) energiát engednek a környezetbe, akkor az entalpia változása (ΔH-ban kifejezve) negatív értékkel bír..
Ellenkező esetben, ha az intézkedés változása pozitív, az tükrözi a környezetből származó hő felszívódását. Emellett a rendszer entalpiás variációjának nagysága a környezetbe vagy a környezetből átvitt energiamennyiség kifejeződése..
Minél nagyobb az AH nagysága, annál nagyobb az energia kibocsátása a rendszerből a környező közegbe.
Ez azért van, mert ezekben a reakciókban az új kapcsolatok létrehozásakor felszabaduló nettó energia nagyobb, mint a linkek töredezettségében használt nettó energia..
A fentiekből arra lehet következtetni, hogy ez a fajta reakció nagyon gyakori, mert a reakció termékei olyan mennyiségű energiát tárolnak a kötésekben, amelyek nagyobbak, mint a reaktánsokban..
típus
Különböző típusú exoterm reakciók vannak a kémia különböző területein, akár a laboratóriumban, akár az iparágban; némelyiket spontán módon hajtják végre, másoknak szükségük van speciális feltételekre, vagy valamilyen típusú anyagra, mint például a katalizátor előállítására.
Az exoterm reakciók legfontosabb típusai a következők:
Égési reakciók
Az égési reakciók azok a redox típusúak, amelyek akkor lépnek fel, amikor egy vagy több anyag oxigénnel reagál, általában a fény és a hőenergia felszabadulásához, azaz a fényhez és a hőhöz, amikor láng keletkezik..
Semlegesítési reakciók
A semlegesítési reakciókat egy savfaj és egy lúgos anyag (bázis) kölcsönhatása jellemzi, hogy sót és vizet képezzenek, amely exoterm jellegű..
Oxidációs reakciók
Sok ilyen típusú reakció létezik, amelyek exoterm viselkedést mutatnak, mert az oxigén oxidációja nagy mennyiségű energia felszabadulását eredményezi, mint a szénhidrogének oxidációjában..
Termit reakció
Ez a reakció körülbelül 3000 ° C-os hőmérsékletet eredményezhet, és az alumíniumpor nagy mennyiségű fém-oxidokkal való nagy affinitása miatt az acél és a vas hegesztéséhez használják..
Polimerizációs reakció
Ez a fajta reakció az, amely akkor keletkezik, amikor egy bizonyos számú kémiai anyagot neveznek monomereknek, amelyek együttesek, amelyek kombinálva ismétlődnek a láncokban, hogy makromolekuláris szerkezeteket képezzenek..
Nukleáris hasadási reakció
Ez az eljárás a nehéz - azaz 200-nál nagyobb tömegszámú (A) tömegű atom atommagjainak megosztására utal - kisebb méretű közbenső tömegű fragmentumok vagy magok előállítására..
Ebben a reakcióban, ahol egy vagy több neutron keletkezik, nagy mennyiségű energiát szabadít fel, mert a nagyobb tömegű mag alacsonyabb stabilitással rendelkezik, mint a termékei.
Egyéb reakciók
Vannak más nagy jelentőségű exoterm reakciók is, mint például néhány szénhidrát dehidratálása kénsavval való reagáltatással, a szabad levegőnek kitett víz felszívódása vagy a fém fajok oxidációja számos korróziós reakcióban.
Példák
Az alábbiakban néhány példát mutatunk be az exoterm reakciókra, amelyek az entalpia változását eredményezik, ami negatív értékkel bír, mivel az energiát felszabadítja, amint azt fentebb említettük..
Például a propán égése spontán exoterm reakció:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Az exoterm viselkedés másik esetét a nátrium-karbonát és a sósav közötti semlegesítési reakció mutatja:
nátrium-hidrogén3(ac) + HCI (ac) → NaCl (ac) + H2O (l) + CO2(G)
Ismertetjük az etanol ecetsavvá történő oxidálását is, amely teljes reakcióját a következő egyenlet mutatja:
3CH3CH2OH + 2K2Cr2O7 + 8H2SW4 → CH3COOH + 2Cr (SO4)3 + 2K2SW4 + 11H2O
Az exoterm reakció egy másik osztálya az úgynevezett termitikus reakció, amelyben az alumíniumot egy fém-oxiddal kombináljuk, amint azt az alábbi példákban mutatjuk be:
2Al (ok) + hit2O3→ Al2O3(s) + Fe (l)
A fentiekben ismertetett példákon túlmenően számos olyan reakció létezik, amelyek szintén exotermnek tekinthetők, mint például bizonyos szerves hulladékok komposztálásra történő bomlása..
Emellett kiemeli a luciferin pigment oxidálódását a luciferáz enzim hatásával, hogy sokféle reakcióban termelje a szentjánosbogarakra jellemző biolumineszcenciát, sőt még légzést is..
referenciák
- Wikipedia. (N.d.). Exoterm reakció. A (z) es.wikipedia.org webhelyről származik
- BBC. (N.d.). Energia változások és reverzibilis reakciók. A bbc.co.uk-ból származik
- Chang, R. (2007). Kémia, kilencedik kiadás. (McGraw-Hill).
- Walker, D. (2007). Kémiai reakciók. A következőt kapta: books.google.co.ve
- Saunders, N. (2007). Kémiai reakciók feltárása. A következőt kapta: books.google.co.ve


