Kalcium-oxid (CaO) szerkezete, tulajdonságai és felhasználása
az kalcium-oxid (CaO) egy szervetlen vegyület, amely ionos formában kalciumot és oxigént tartalmaz (nem szabad összekeverni a kalcium-peroxiddal, CaO-val).2). Világszerte lime néven ismert, amely olyan szervetlen vegyületet jelöl, amely karbonátokat, kalcium-oxidokat és -hidroxidokat, valamint más fémeket, például szilíciumot, alumíniumot és vasat tartalmaz..
Ezt az oxidot (vagy mészet) közönséges nyelvként is említjük, mint a mész vagy a lecsapott mész, attól függően, hogy hidratált-e vagy sem. A mész kalcium-oxid, míg a hideg mész a hidroxid. A mészkő (mészkő vagy keményített mész) tulajdonképpen egy főleg kalcium-karbonátból álló üledékes kőzet (CaCO).3).

A kalcium egyik legnagyobb természetes forrása, és a nyersanyag a kalcium-oxid előállításához. Hogyan keletkezik ez az oxid? A karbonátok érzékenyek a termikus bomlásra; a kalcium-karbonátok 825 ° C feletti hőmérsékleten történő melegítése, amely mész és szén-dioxid képződéséhez vezet.
A fenti állítás a következőképpen írható le: CaCO3→ CaO (k) + CO2(G). Mivel a földkéreg mészkőben és kalcitban gazdag, az óceánokban és a strandokban pedig bőséges tengeri kagyló (nyersanyagok a kalcium-oxid előállításához), a kalcium-oxid viszonylag olcsó reagens.
index
- 1 Formula
- 2 Szerkezet
- 3 Tulajdonságok
- 3.1 Oldhatóság
- 4 Felhasználások
- 4.1 Habarcsként
- 4.2 A szemüveg gyártása
- 4.3 A bányászatban
- 4.4 Szilikát eltávolító
- 5 Kalcium-oxid nanorészecskék
- 6 Referenciák
képlet
A kalcium-oxid kémiai képlete CaO, amelyben a kalcium hasonlít a savionhoz (elektron-akceptor) Ca2+, és oxigént, mint bázikus iont (elektron donor) VAGY2--.
Miért töltik fel a kalcium +2-t? Mivel a kalcium a periodikus táblázat (Mr. Becambara) 2. csoportjába tartozik, és csak két valenselektron áll rendelkezésre a kötések kialakításához, amelyek az oxigénatomhoz jutnak.
struktúra
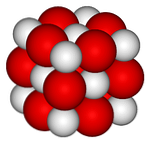
A felső képen a kalcium-oxid kristályos szerkezete (gem-salt type) látható. A terjedelmes piros gömbök megfelelnek a Ca ionoknak2+ és a fehér gömböket az ionokhoz2-.
Ebben a köbös kristály elrendezésben minden ion Ca2+ hat ion van körülvéve O2-, elzáródtak a nagy ionok között maradt oktaéderes lyukak között.
Ez a szerkezet ennek az oxidnak a maximális ionos jellegét fejezi ki, bár a sugárok jelentős különbsége (a piros gömb nagyobb, mint a fehér) gyengébb kristályos retikuláris energiát biztosít a MgO-hoz képest..
tulajdonságok
Fizikailag ez egy kristályos fehér szilárd anyag, szagtalan és erős elektrosztatikus kölcsönhatásokkal, amelyek felelősek a magas olvadáspontokért (2572 ° C) és forrásig (2850 ° C). Emellett a molekulatömege 55,958 g / mol, és az érdekes tulajdonsága, hogy termolumineszcens.
Ez azt jelenti, hogy egy lángnak kitett kalcium-oxid egy intenzív fehér fénygel ragyoghat, melyet angolul ismertek. rivaldafény, vagy spanyolul, kalciumfény. A Ca ionok2+, a tűzzel érintkezve vöröses lángot okoznak, amint az a következő képen látható.

oldhatóság
A CaO egy bázikus oxid, amelynek erős affinitása van a vízzel, olyan mértékben, hogy abszorbeálja a nedvességet (higroszkópos szilárd anyag), azonnal reagál a hígított mész vagy kalcium-hidroxid előállítására:
CaO (s) + H2O (l) => Ca (OH)2(S)
Ez a reakció exoterm (a hőt kibocsátja) erősebb kölcsönhatásokkal és stabilabb kristályrácsokkal rendelkező szilárd anyag képződése miatt. A reakció azonban reverzibilis, ha Ca (OH) -ot melegítünk2, dehidratálják és megvilágítják a lecsapott mészet; akkor a mész "újjászületett".
A kapott oldat nagyon bázikus, és ha kalcium-oxiddal telített, akkor a pH-értéke 12,8.
Hasonlóképpen oldható glicerinben és sav- és cukoroldatokban. Mivel ez egy bázikus oxid, természetesen hatékony kölcsönhatás van a savas oxidokkal (SiO2, az2O3 és a hit2O3, például a folyékony fázisban oldható. Másrészt alkoholokban és szerves oldószerekben oldhatatlan.
alkalmazások
A CaO számos ipari felhasználással, valamint acetilén szintézisével (CH≡CH) rendelkezik a foszfátok szennyvízből történő extrakciójában és a gáz halmazállapotú hulladékból származó kén-dioxiddal való reakcióban..
A kalcium-oxid egyéb felhasználását az alábbiakban ismertetjük:
Habarcsként
Ha a kalcium-oxidot homokkal keverjük (SiO2) és a víz, sütjük a homokkal, és lassan reagál a vízzel, hogy szétzúzott mész képződjön. A CO2 a levegő feloldódik a vízben és reagál a sóval, hogy kalcium-karbonát képződjön:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2O (l)
A CaCO3 Ez egy ellenállóbb és keményebb vegyület, mint a CaO, ami a habarcsot (az előző keveréket) megkeményíti és rögzíti a téglákat, tömböket vagy kerámiákat közöttük vagy a kívánt felületre.
A szemüveg gyártása
A szemüveg előállításához az alapvető nyersanyag a szilícium-oxidok, amelyek mészrel, nátrium-karbonáttal (Na2CO3) és egyéb adalékanyagok, amelyeket melegítésnek vetünk alá, így üveges szilárd anyagot kapunk. Ezt a szilárd anyagot ezután bármilyen számban melegítjük és fújjuk.
A bányászatban
A hidrogénkötés (O-H-O) kölcsönhatások következtében a lecsapott mész nagyobb mennyiséget foglal el, mint a mész. Ezt a tulajdonságot arra használják, hogy a sziklákat belülről megtörje.
Ezt úgy érik el, hogy a mész és a víz egy kompakt keverékével tölti őket, amely a hőt és a táguló erőt a sziklára fókuszálja..
Mint szilikát eltávolító
A CaO-t a szilikátokkal olvasztottuk össze, hogy koaleszcens folyadékot képezzünk, amelyet azután egy adott termék nyersanyagából extrahálunk.
Például a vasércek a fém vas és acél előállításának alapanyaga. Ezek az ásványok szilikátokat tartalmaznak, amelyek a folyamat nemkívánatos szennyeződései, és a fent leírt módszerrel eliminálódnak.
Kalcium-oxid nanorészecskék
A kalcium-oxid nanorészecskékként szintetizálható, megváltoztatva a kalcium-nitrát koncentrációját (Ca (NO)3)2) és nátrium-hidroxid (NaOH) oldatban.
Ezek a részecskék gömb alakúak, bázikusak (valamint a makroszintű szilárd anyagok), és sok felületük van. Következésképpen ezek a tulajdonságok előnyösek a katalitikus folyamatok számára. Mi az? A vizsgálatok jelenleg válaszolnak erre a kérdésre.
Ezeket a nanorészecskéket alkalmazták a piridinekből származó szubsztituált szerves vegyületek szintetizálására új gyógyszerkészítmények előállításában, olyan kémiai átalakítások elvégzésére, mint a mesterséges fotoszintézis, a nehéz és mérgező fémek víz tisztítására, és fotokatalitikus szerek.
A nanorészecskéket biológiai hordozón szintetizálhatjuk, mint például a papaya és a zöld tea levelei, amelyeket antibakteriális szerként használnak..
referenciák
- scifun.org. (2018). Mész: kalcium-oxid. 2018. március 30-án, a következő címen szerezhető be: scifun.org.
- Wikipedia. (2018). Kalcium-oxid. 2018 március 30-án, az alábbi címen szerezhető be: en.wikipedia.org
- Ashwini Anantharaman és mtsai. (2016). A kalcium-oxid nanorészecskék és alkalmazásai zöld szintézise. Int. Journal of Engineering Research and Application. ISSN: 2248-9622, 6. kötet, 10. kiadás (-1. Rész), 27-31.
- J. Safaei-Ghomi és mtsai. (2013). Kalcium-oxid nanorészecskék katalizálják az egylépéses, nagy szubsztitúciójú piridinek szintetizálását vizes etanol közegben, a Scientia Iranica, C tranzakciók: kémia és kémiai technika 20 549-554.
- Pubchem. (2018). Kalcium-oxid. 2018 március 30-án, a következő címen szerezhető be: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Szervetlen kémia -ban A 2. csoport elemei. (negyedik kiadás, 280. oldal). Mc Graw-hegy.


