ATP (adenozin-trifoszfát) szerkezet, funkciók, hidrolízis
az ATP (adenozin-trifoszfát) egy nagy molekulatömegű szerves molekula, amely egy adenin gyűrűből, egy ribózból és három foszfátcsoportból áll. Alapvető szerepe van az anyagcserében, mivel szállítja a szükséges energiát a hatékony sejtek működésének fenntartásához.
Az "energia pénznem" kifejezést széles körben ismerik, mivel kialakulása és használata könnyen előfordul, lehetővé téve, hogy gyorsan fizessenek az energiát igénylő kémiai reakciókra.
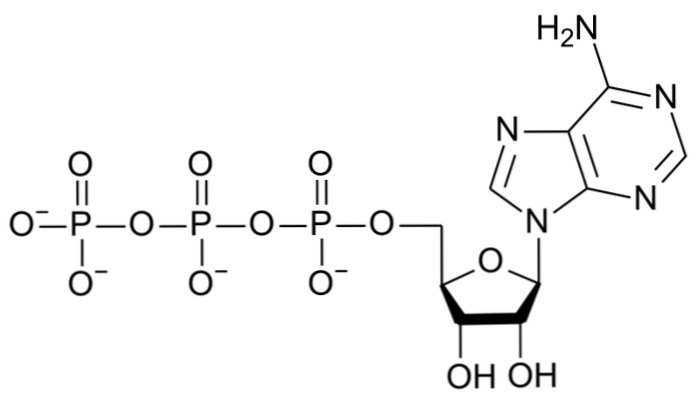
Bár a szabad szemmel rendelkező molekula kicsi és egyszerű, jelentős mennyiségű energiát takarít meg kapcsolataiban. A foszfátcsoportok negatív töltésekkel rendelkeznek, amelyek állandó repulzióval rendelkeznek, így labilis és könnyen törhető linket alkotnak.
Az ATP hidrolízise a molekula lebontása víz jelenlétével. Ezzel a folyamaton keresztül a szabad energiát szabadítják fel.
Az ATP-nek két fő forrása van: a szubsztrát szintjén a foszforiláció és az oxidatív foszforiláció, az utóbbi pedig a legfontosabb és leggyakrabban használt sejt..
Az oxidatív foszforiláció összekapcsolja az FADH oxidációját2 és az NADH + H+ a mitokondriumokban és a szubsztrát szintjén a foszforiláció az elektronátviteli láncon kívül történik, olyan útvonalakon, mint a glikolízis és a trikarbonsav ciklus.
Ez a molekula felelős a energiához, amely a sejten belüli folyamatok többségéhez szükséges, a fehérjeszintézistől a mozgásig. Ezenkívül lehetővé teszi a molekulák forgalmát a membránokon keresztül, és a sejtjelzésre hat.
index
- 1 Szerkezet
- 2 Funkciók
- 2.1 Energiaellátás a nátrium és a kálium membránon való szállítására
- 2.2 A fehérjeszintézisben való részvétel
- 2.3 Energiaellátás a mozgáshoz
- 3 Hidrolízis
- 3.1 Miért következik be ez az energiaszabadulás?
- 4 Az ATP beszerzése
- 4.1 Oxidatív foszforiláció
- 4.2 Foszforiláció a szubsztrát szintjén
- 5 ATP ciklus
- 6 Egyéb energiamolekulák
- 7 Referenciák
struktúra
Az ATP a neve szerint három foszfátot tartalmazó nukleotid. Különleges szerkezete, különösképpen a két pirofoszfátkötés, ez energiában gazdag vegyület. A következő elemekből áll:
- Egy nitrogénbázis, adenin. A nitrogénbázisok olyan gyűrűs vegyületek, amelyek szerkezetükben egy vagy több nitrogént tartalmaznak. A nukleinsavak, a DNS és az RNS komponensei is megtalálhatók.
- A ribóz a molekula közepén helyezkedik el. Ez egy pentóz típusú cukor, mivel öt szénatomot tartalmaz. Kémiai képlete C5H10O5. A ribóz szénatomja az adenin gyűrűhöz kapcsolódik.
- Három foszfátcsoport. Az utolsó kettő a "nagy energiájú kapcsolatok", és a grafikus struktúrákban a virgulilla szimbólumával vannak ábrázolva: ~. A foszfátcsoport a biológiai rendszerekben az egyik legfontosabb. A három csoportot a legközelebbi legközelebbi alfa, béta és gamma nevezik.
Ez a kapcsolat nagyon labilis, így gyorsan, egyszerűen és spontán módon oszlik meg, amikor a szervezet élettani feltételei megkövetelik. Ez azért fordul elő, mert a három foszfátcsoport negatív töltése folyamatosan próbál elmozdulni egymástól.
funkciók
Az ATP-nek nélkülözhetetlen szerepe van a gyakorlatilag minden élő szervezet energia-anyagcseréjében. Emiatt gyakran nevezik energia pénznemnek, mivel néhány perc alatt folyamatosan tölthető és feltölthető..
Közvetlen vagy közvetett, az ATP biztosítja a több száz folyamat energiáját, amellett, hogy foszfát donorként működik.
Általában az ATP jelző molekulaként működik a sejten belüli folyamatokban, a DNS és az RNS komponenseinek szintetizálásához és más biomolekulák szintéziséhez szükséges. többek között a membránok.
Az ATP felhasználása főbb kategóriákra osztható: molekulák szállítása biológiai membránokon keresztül, különböző vegyületek szintézise és végül mechanikai munka..
Az ATP funkciói nagyon szélesek. Ráadásul olyan sok reakcióban vesz részt, hogy lehetetlen lenne megnevezni őket. Ezért három konkrét példát fogunk megvitatni a három említett felhasználás példáinak bemutatására.
Energiaellátás a nátrium és a kálium membránon keresztüli szállítására
A sejt egy rendkívül dinamikus környezet, amely megköveteli a specifikus koncentrációk fenntartását. A legtöbb molekula véletlenszerűen vagy véletlenül nem lép be a sejtbe. Ahhoz, hogy egy molekula vagy anyag beléphessen, ezt az adott szállítónak meg kell tennie.
A transzporterek olyan fehérjék, amelyek áthaladnak a membránon, és celluláris "átjáróként" működnek, és szabályozzák az anyagok áramlását. Ezért a membrán féligáteresztő: lehetővé teszi bizonyos vegyületek bejutását és mások nem.
Az egyik legismertebb szállítás a nátrium-kálium-szivattyú. Ez a mechanizmus aktív szállításnak minősül, mivel az ionok mozgása a koncentrációjukkal ellentétes, és az egyetlen módja annak, hogy ezt a mozgást végrehajtsuk az energia bevezetése a rendszerbe, ATP formájában..
Becslések szerint a cellában kialakított ATP egyharmadát a szivattyú aktív tartására használják. A nátriumionokat állandóan szivattyúzzák a sejt külsejébe, míg a káliumionok fordítva fordulnak elő.
Logikusan az ATP használata nem korlátozódik a nátrium és a kálium szállítására. Vannak más ionok, mint például a kalcium, a magnézium, amelyeknek ezt az energia pénznemet kell belépniük.
A fehérjeszintézisben való részvétel
A fehérje molekulákat aminosavak képezik, amelyeket peptidkötések kötnek össze. Ezek megalkotásához négy nagy energiájú kötés törése szükséges. Más szavakkal, jelentős számú ATP-molekulát hidrolizálni kell egy átlagos hosszúságú fehérje képződéséhez.
A fehérjék szintézise a riboszómáknak nevezett struktúrákban történik. Képesek értelmezni a hírvivő RNS által kódolt kódot és egy aminosav-szekvenciává, az ATP-függő folyamatba fordítani..
A legaktívabb sejtekben a fehérjeszintézis az ATP szintézisének 75% -át képes irányítani.
Másrészről a sejt nemcsak fehérjéket szintetizál, hanem lipideket, koleszterint és más nélkülözhetetlen anyagokat is igényel, és ehhez az ATP kötésekben lévő energiát igényli..
Adjon energiát a mozgáshoz
A mechanikai munka az ATP egyik legfontosabb funkciója. Például ahhoz, hogy testünk képes legyen az izomrostok összehúzódására, nagy mennyiségű energia rendelkezésre állása szükséges.
Az izomban a kémiai energia átalakulhat mechanikai energiává az általa képződő kontrakciós kapacitású fehérjék átszervezésének köszönhetően. Ezeknek a szerkezeteknek a hosszát módosítják, lerövidítik, ami feszültséget eredményez, ami a mozgás keletkezéséhez vezet.
Más szervezetekben a sejtek mozgása az ATP jelenlétének köszönhetően is előfordul. Például az egyes egysejtű organizmusok elmozdulását lehetővé tevő csillogás és zászlórúd mozgása az ATP használatával történik..
Egy másik konkrét mozgás az amoebic, amely magában foglalja a pszeudopod kiemelkedését a sejt végén. Számos sejttípus használja ezt a mozgási mechanizmust, beleértve a leukocitákat és a fibroblasztokat.
A csírasejtek esetében a mozgás elengedhetetlen az embrió hatékony fejlődéséhez. Az embrionális sejtek jelentős távolságokat mozgatnak a származási helyüktől a régióhoz, ahol meghatározott struktúrákból kell származniuk.
hidrolízis
Az ATP hidrolízise olyan reakció, amely a molekula vízzel való lebontásával jár. A reakciót a következőképpen mutatjuk be:
ATP + víz ⇋ ADP + Pén + energiát. Hol van a P kifejezésén a szervetlen foszfát csoportjára vonatkozik, és az ADP az adenozin-difoszfát. Vegye figyelembe, hogy a reakció reverzibilis.
Az ATP hidrolízise olyan jelenség, amely hatalmas mennyiségű energiát bocsát ki. A pirofoszfátkötések bármelyikének megszakadása 7 kcal / mól-specifikusan 7,3% ATP-t eredményez az ADP-re és 8,2 az ATP-ből származó adenozin-monofoszfát (AMP) előállítására. Ez 12 000 kalóriát jelent az ATP móljára számítva.
Miért következik be ez az energiaszabadulás??
Mivel a hidrolízis termékei sokkal stabilabbak, mint a kezdeti vegyület, azaz az ATP.
Meg kell említeni, hogy csak a pirofoszfát kötéseken keletkező hidrolízis, amely az ADP vagy AMP kialakulásához vezet, jelentős mennyiségű energiatermeléshez vezet..
A molekulában lévő többi kötés hidrolízise nem nyújt annyi energiát, kivéve a szervetlen pirofoszfát hidrolízisét, amely nagy mennyiségű energiával rendelkezik..
Az ezekből a reakciókból származó energia felszabadulását a sejten belüli metabolikus reakciók végrehajtására használják, mivel sok ilyen eljárás energiát igényel, mind a lebomlási útvonalak kezdeti lépéseiben, mind a vegyületek bioszintézisében..
Például a glükóz anyagcserében a kezdeti lépések a molekula foszforilációját foglalják magukban. A következő lépésekben új ATP keletkezik, hogy pozitív nettó nyereséget kapjunk.
Energetikai szempontból más molekulák is vannak, amelyek energia-felszabadulása nagyobb, mint az ATP, beleértve az 1,3-bifoszfoglicerátot, a karbamil-foszfátot, a kreatinin-foszfátot és a foszfoinol-piruvátot..
Az ATP beszerzése
Az ATP-t két módon lehet előállítani: oxidatív foszforiláció és foszforiláció a szubsztrát szinten. Az elsőnek oxigénre van szüksége, míg a másodiknak nincs szüksége rá. A kialakult ATP körülbelül 95% -a a mitokondriumokban fordul elő.
Oxidatív foszforiláció
Az oxidatív foszforiláció során a tápanyagok két fázisban oxidálódnak: csökkentett koenzimek NADH és FADH előállítása2 vitaminok származékai.
Ezeknek a molekuláknak a csökkentése megköveteli a tápanyagok hidrogének használatát. A zsírokban a koenzimek előállítása figyelemre méltó, köszönhetően a szerkezetükben lévő óriási mennyiségű hidrogénnek a peptidekkel vagy szénhidrátokkal összehasonlítva..
Bár számos módja van a koenzimek előállításának, a legfontosabb út a Krebs-ciklus. Ezt követően a redukált koenzimek koncentrálódnak a mitokondriumokban található légzési láncokban, amelyek az elektronokat oxigénbe szállítják..
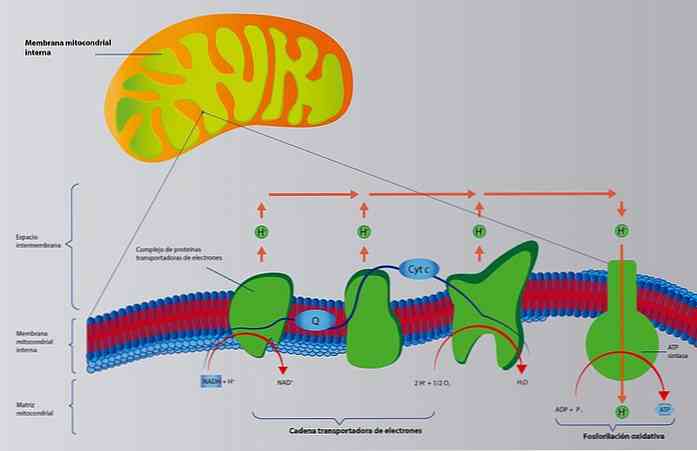
Az elektronátviteli láncot a membránhoz kapcsolt fehérjék sora alkotja, amelyek a protonokat (H +) a külső oldalra pumpálják (lásd a képet). Ezek a protonok ismét áthaladnak a membránon egy másik, ATP-szintézisért felelős fehérje, ATP-szintáz segítségével.
Más szavakkal, csökkentenünk kell a koenzimeket, több ADP-t és oxigént termelnek víz és ATP.
Foszforiláció a szubsztrát szintjén
A szubsztrát szintjén a foszforiláció nem olyan fontos, mint a fent leírt mechanizmus, és mivel nem igényel oxigénmolekulákat, általában a fermentációhoz kapcsolódik. Ily módon, bár nagyon gyors, kevés energiát nyer ki, ha összehasonlítjuk az oxidációs eljárással, akkor tizenöt alkalommal kevesebb lenne.
Testünkben az erjedési folyamatok az izom szintjén fordulnak elő. Ez a szövet oxigén nélkül működhet, így lehetséges, hogy egy glükózmolekula tejsavvá lebomlik (ha például kimerítő sporttevékenységet végzünk).
Az erjesztések során a végtermék még mindig energiamegtakarítással rendelkezik, amely kivonható. Az izomban történő erjedés esetén a tejsavban lévő szénatomok ugyanolyan mértékű csökkenést mutatnak, mint a kezdeti molekulában: glükóz.
Így az energiatermelés olyan molekulák képződésével történik, amelyek nagy energiájú kötéseket tartalmaznak, beleértve az 1,3-bifoszoglirátot és a foszfonol-piruvátot..
Glikolízisben például ezeknek a vegyületeknek a hidrolízise az ATP molekulák termeléséhez kapcsolódik, így a "szubsztrátszint" kifejezés..
ATP ciklus
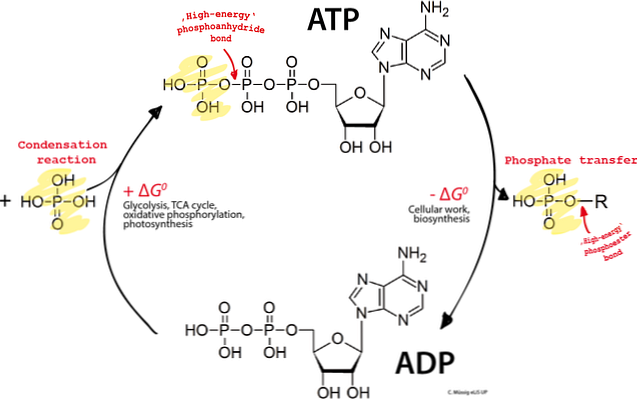
Az ATP-t soha nem tárolja. Folyamatos ciklusban és szintézisben van. Ily módon egyensúly alakul ki a kialakult ATP és a hidrolizált termék, az ADP között.
Más energiamolekulák
Az ATP nem az egyetlen olyan molekula, amely a celluláris metabolizmusban létező nukleozid bifoszfátból áll. Vannak olyan molekulák, amelyek hasonlóak az ATP-hez hasonló struktúrákkal, amelyek hasonló energia viselkedéssel rendelkeznek, bár nem olyan népszerűek, mint az ATP.
A legkiválóbb példa a GTP, a guanozin-trifoszfát, amelyet az ismert Krebs-ciklusban és a glükoneogén útban használnak. Mások kevésbé használtak a CTP, TTP és UTP.
referenciák
- Guyton, A. C. és Hall, J. E. (2000). Az emberi fiziológia tankönyve.
- Hall, J. E. (2017). Guyton E Hall Gyógymód az orvosi fiziológiáról. Elsevier Brazília.
- Hernandez, A. G. D. (2010). Táplálkozási szerződés: az élelmiszer összetétele és táplálkozási minősége. Ed. Panamericana Medical.
- Lim, M. Y. (2010). Az anyagcsere és a táplálkozás lényege. Elsevier.
- Pratt, C. W., és Kathleen, C. (2012). biokémia. Szerkesztői The Modern Manual.
- Voet, D., Voet, J. G. és Pratt, C. W. (2007). A biokémia alapjai. Orvosi szerkesztői Panamericana.


