Etil-acetát szerkezet, tulajdonságok, szintézis, felhasználások és kockázatok
az etil-acetát vagy etil-etanoát (IUPAC név) egy szerves vegyület, amelynek kémiai képlete CH3COO2H5. Egy észterből áll, ahol az alkohol komponens etanolból származik, míg karbonsavkomponense ecetsavból származik.
Ez a folyadék normál hőmérsékleti és nyomásfeltételek mellett kellemes aromát mutat a gyümölcsök számára. Ez a tulajdonság tökéletesen illeszkedik az észterből elvárt elvárásokhoz; ami az etil-acetát kémiai jellege. Emiatt az élelmiszerekben és az alkoholtartalmú italokban használatos.
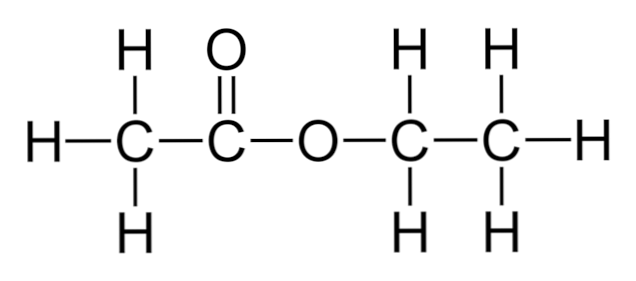
A felső képen az etil-acetát szerkezeti váza látható. Jegyezzük meg a bal oldali karbonsavkomponensét, és jobbra az alkohol komponenst. Strukturális szempontból várható, hogy ez a vegyület úgy viselkedik, mint az ecet és az alkohol közötti hibrid; azonban saját tulajdonságai vannak.
Ez az, ahol az észtereknek nevezett ilyen hibridek különböznek egymástól. Az etil-acetát savként nem reagál, és OH-csoport hiányában sem dehidratálhat. Ehelyett erős bázis, például nátrium-hidroxid, NaOH jelenlétében bázikus hidrolízist végez.
Ezt a hidrolízisreakciót a kémiai kinetikai kísérletekhez használt laboratóriumokban használják; ahol a reakció továbbá másodrendű. Hidrolízis bekövetkezésekor gyakorlatilag az etil-etanoát visszatér a kezdeti komponenseihez: sav (NaOH-val deprotonálva) és alkohol.
Szerkezeti vázában megfigyelhető, hogy a hidrogénatomok az oxigén felett dominálnak. Ez befolyásolja azoknak a képességét, hogy kölcsönhatásba lépjenek a nem poláros fajokkal, például a zsírokkal. Alkalmazható olyan vegyületek, mint például gyanták, festékek és általában szerves szilárd anyagok oldására is.
Annak ellenére, hogy kellemes aromája van, a folyadék hosszabb ideig tartó expozíciója negatív hatást fejt ki (mint a szinte minden kémiai vegyület) a szervezetben.
index
- 1 Az etil-acetát szerkezete
- 1.1 A hidrogén donor atomok hiánya
- 2 Fizikai és kémiai tulajdonságok
- 2.1 Nevek
- 2.2 Molekuláris képlet
- 2.3 Molekulatömeg
- 2.4 Fizikai leírás
- 2.5 Szín
- 2.6 Illat
- 2.7 Íz
- 2.8 Szagküszöb
- 2.9 Forráspont
- 2.10 Olvadáspont
- 2.11 Oldhatóság vízben
- 2.12 Oldhatóság szerves oldószerekben
- 2.13 Sűrűség
- 2.14 Gőzsűrűség
- 2.15 Stabilitás
- 2.16 Gőznyomás
- 2.17 Viszkozitás
- 2.18 Az égési hő
- 2.19 Párolgási hő
- 2.20 Felületi feszültség
- 2.21 Refraktív index
- 2.22 Tárolási hőmérséklet
- 2.23 pKa
- 3 Összefoglalás
- 3.1 Fisher reakciója
- 3.2 Tishchenko reakció
- 3.3 Egyéb módszerek
- 4 Felhasználások
- 4.1 Oldószer
- 4.2 Mesterséges ízek
- 4.3 Analytics
- 4.4 Szerves szintézis
- 4.5 Kromatográfia
- 4.6 Entomológia
- 5 Kockázatok
- 6 Referenciák
Az etil-acetát szerkezete
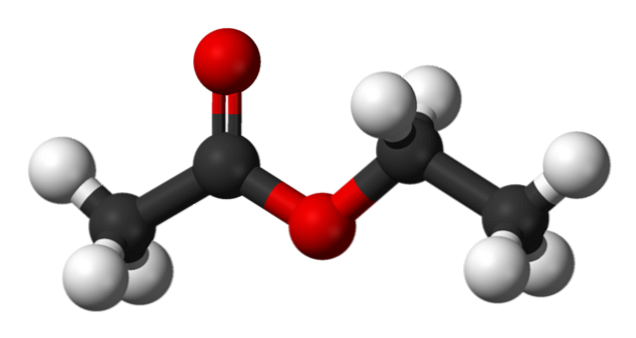
A felső képen az etil-acetát szerkezetét a gömbök és a rudak modellje mutatja. Ebben a modellben kiemelték a vörös gömbökkel rendelkező oxigénatomokat; balra a savból származó frakció, és jobbra az alkoholból (alkoxicsoport, -OR) származó frakció..
A karbonilcsoportot a C = O kötés (a kettős rudak) értékelik. A csoport körüli szerkezet és a szomszédos oxigén sík, mivel mindkét oxigén közötti rezonanciával a terhelés áthelyeződik; az a-hidrogén viszonylag alacsony savtartalmának magyarázata (a -CH-csoporté)3, kapcsolódik C = O).
A molekula két kötésének elforgatásával közvetlenül segíti, hogy kölcsönhatásba lépjen más molekulákkal. A két oxigénatom jelenléte és az aszimmetria a struktúrában állandó dipol pillanatot ad; amely viszont a dipol-dipol kölcsönhatásáért felelős.
Például az elektronikus sűrűség nagyobb a két oxigénatom közelében, jelentősen csökken a -CH csoportban3, és fokozatosan az OCH csoportban2CH3.
Ezen kölcsönhatások miatt az etil-acetát molekulák normál körülmények között folyadékot képeznek, amely jelentősen magas forrásponttal rendelkezik (77 ° C)..
A hidrogénkötések donor atomjainak hiánya
Ha közelebbről megnézzük a struktúrát, észre fogod venni, hogy nincs atom, amely képes hidrogénhíd adományozására. Az oxigénatomok azonban ilyen akceptorok, és az etil-acetát vízben nagyon jól oldódik, és jelentős mértékben kölcsönhatásba lép a poláris vegyületekkel és a hidrogénkötésű donorokkal (például cukrokkal)..
Ez is lehetővé teszi, hogy kiválóan vegyen részt az etanollal; ezért nem meglepő az alkoholos italokban való jelenléte.
Másrészt, az alkoxicsoportja lehetővé teszi, hogy bizonyos apoláris vegyületekkel, például kloroformmal, CH-val kölcsönhatásba lépjen3Cl.
Fizikai és kémiai tulajdonságok
nevek
-Etil-acetát
-Etil-etanoát
-Ecetsav-észter
-Acetoxietano
Molekuláris képlet
C4H8O2 vagy CH3COO2H5
Molekulatömeg
88,106 g / mol.
Fizikai leírás
Tiszta, színtelen folyadék.
szín
Színtelen folyadék.
szag
Jellemző az éterekre, hasonlóan az ananász illatához.
aroma
Kellemes, ha hígítjuk, gyümölcsös ízt ad a sörnek.
Szagküszöb
3,9 ppm. 0,0196 mg / m3 (alacsony szag); 665 mg / m3 (magas szag).
Az érzékelhető szag 7 - 50 ppm (átlag = 8 ppm).
Forráspont
171–760 Hgmm (77,1 ° C).
Olvadáspont
-118,5 ° F (-83,8 ° C).
Oldhatóság vízben
80 g / l.
Oldhatóság szerves oldószerekben
Etil- és etil-éterrel elegyedik. Nagyon jól oldódik acetonban és benzolban. Kloroformmal, rögzített és illékony olajokkal, valamint oxigénnel és klórozott oldószerekkel elegyíthető.
sűrűség
0,9003 g / cm33.
Gőzsűrűség
3.04 (levegő arány: 1).
stabilitás
Lassan bomlik nedvességgel; több műanyaggal és erős oxidálószerrel összeegyeztethetetlen. A keverék vízzel robbanásveszélyes lehet.
Gőznyomás
93,2 mmHg 25 ° C-on
viszkozitás
0,423 mPoise 25 ° C-on.
Az égési hő
2,238,1 kJ / mol.
Párolgási hő
35,60 kJ / mol 25 ° C-on.
Felületi feszültség
24 din / cm 20 ° C-on.
Törésmutató
1,373 ° C-on / ° C-on.
Tárolási hőmérséklet
2 - 8 ° C.
pKa
16 - 18 ° C-on 25 ° C-on.
szintézis
Fisher reakciója
Az etil-acetátot ipari módszerrel szintetizáljuk Fisher-reakcióval, amelyben etanolt ecetsavval észterezünk. A reakciót szobahőmérsékleten hajtjuk végre.
CH3CH2OH + CH3COOH <=> CH3COOCH2CH3 + H2O
A reakciót savkatalízissel gyorsítjuk. Az egyensúly jobbra mozog, azaz az etil-acetát előállítása felé a víz eltávolításával; a tömeges cselekvési törvény szerint.
Tishchenko reakciója
Etil-acetátot is előállítunk ipari úton a Tishchenko-reakció alkalmazásával, két ekvivalens acetaldehidet konjugálva egy alkoxid alkalmazásával katalizátorként..
2 CH3CHO => CH3COOCH2CH3
Egyéb módszerek
-Az etil-acetátot a bután ecetsavvá történő oxidációjával előállítjuk, 175 ° C-on és 50 atm nyomáson végzett reakcióban. Kobalt- és krómionokat használnak katalizátorként.
-Az etil-acetát a polivinil-acetát és a polivinil-alkohol etanolízisének együttes terméke.
-Etil-acetátot állít elő az iparban az etanol dehidrogénezésével is, a reakciót a réz alkalmazása megemelt hőmérsékleten, de 250 ° C-nál kisebb mértékben katalizálja..
alkalmazások
oldószer
Etil-acetátot használnak oldószerként és hígítószerként, amelyet az áramköri lapok tisztítására használnak. Oldószerként használják a módosított komlókivonat előállításához, valamint a kávé és a tea leveleinek koffeinmentesítéséhez. A gyümölcsök és zöldségek jelölésére használt tintákban használatos.
A textiliparban etil-acetátot használnak tisztítószerként. A cukrok szétválasztásánál használt hőmérők kalibrálására használják. A festékiparban oldószerként és oldószerként használják fel a felhasznált anyagokat.
Mesterséges ízek
A gyümölcsízek kidolgozására használják; Például: banán, körte, őszibarack és ananász, valamint szőlő aroma stb..
analitikai
A bizmut, a bór, az arany, a molibdén és a platina, valamint a tallium oldószer meghatározására használják. Az etil-acetát képes olyan vizes oldatban lévő vegyületek és elemek kivonására, mint például foszfor, kobalt, volfrám és arzén.
Szerves szintézisek
Az etil-acetátot az iparban viszkozitáscsökkentőként alkalmazzuk a fotorezisztens készítményekben alkalmazott gyantákhoz. Ezt acetamid, acetil-acetát és metil-heptanon előállítására használják.
kromatográfia
A laboratóriumokban az oszlopkromatográfiák mozgófázisaként és extrakciós oldószerként etil-acetátot használnak. Ha az etil-acetát viszonylag alacsony forráspontot tartalmaz, könnyen elpárolog, ami lehetővé teszi az oldott anyagok koncentrálását az oldószerben..
rovartan
Etil-acetátot használnak az entomológiában a tartályba helyezett rovarok elfojtására, ami lehetővé teszi a gyűjtést és tanulmányozást. Az etil-acetát gőzei megölik a rovart anélkül, hogy megsemmisítenék, és megakadályozzák annak megszilárdulását, megkönnyítve a gyűjtést.
kockázatok
-Az LD50 Az etil-acetát mennyisége patkányokban alacsony toxicitást mutat. Ez azonban irritálja a bőrt, a szemet, a bőrt, az orrot és a torkot.
-A magas szintű expozíció szédülést és ájulást okozhat. A hosszú távú expozíció befolyásolhatja a máj és a vesét is.
-Az etil-acetát 20 000 - 43 000 ppm koncentrációjú belégzése tüdőödémát és vérzést okozhat.
-A munkahelyi expozíciós határértéket az OSHA a levegőben 400 ppm-nél határozta meg, átlagosan 8 órás munkamenet során.
referenciák
- Steven A. Hardinger. (2017). A szerves kémia illusztrált jelentése: etil-acetát (EtOAc). Lap forrása: chem.ucla.edu
- Graham Solomons T. W., Craig B. Fryhle. (2011). Szerves kémia. Aminok. (10th kiadás.). Wiley Plus.
- Morrison, R. T. és Boyd, R. N. (1990). Szerves kémia (5ta kiadás). Szerkesztői Addison-Wesley Iberoamericana.
- Wikipedia. (2019). Etil-acetát. Lap forrása: en.wikipedia.org
- Cotton S. (s.f.). Etil-acetát. Lap forrása: chm.bris.ac.uk
- Pubchem. (2019). Etil-acetát. Lap forrása: pubchem.ncbi.nlm.nih.gov
- Newseed vegyi anyag. (2018). Az etil-acetát alkalmazása és felhasználása. Lap forrása: foodsweeteners.com
- New Jersey Egészségügyi Főosztálya. (2002). Etil-acetát. [PDF]. A lap eredeti címe: nj.gov


