Butino szerkezet, tulajdonságok és felhasználások
az butin egy kémiai vegyület, amely az alkinok csoportjába tartozik, főleg azzal jellemezve, hogy szerkezetében legalább három kötés van két szénatom között..
Amikor az alkynek megnevezésére vonatkozó szabályokat állapítanak meg, az IUPAC (angol nyelvű rövidítés a Nemzetközi Tiszta és Alkalmazott Kémia Unió számára) megállapította, hogy ugyanazokat használják, mint az alkének esetében..

A két típusú anyag nómenklatúrája közötti alapvető különbség az, hogy az utótag-egy -ra változik, vagy olyan vegyületek esetében, amelyek szerkezete háromszoros kötéssel rendelkezik..
Másrészt, a butin áll kizárólag szén- és hidrogén, valamint kétféle módon: 1-butin, amely gázfázisú körülmények között standard hőmérsékleten és nyomáson (1 atm, 25 ° C); és 2-butin, amely egy faj a folyékony fázisban által termelt kémiai szintézisek.
index
- 1 Kémiai szerkezet
- 1.1 1-butino
- 1.2 2-butin
- 2 Tulajdonságok
- 3 Használat
- 4 Referenciák
Kémiai szerkezet
A butin néven ismert molekula a jelenség a szerkezeti izoméria a helyzetben, amely a jelenléte ezen funkciós csoportok mindkét vegyület, de ezek mindegyikének vannak eltérő helyen a lánc fordul elő.
Ebben az esetben a butino mindkét formája azonos molekuláris képlettel rendelkezik; az 1-butinben azonban a hármas kötés az első számú szénatomban van, míg a 2-butinben a második. Ez átalakítja őket pozíció izomerekké.
Mivel a helyét a hármas kötés az egyik a terminálok a szerkezet 1-butin, ez tekinthető egy terminális alkin, míg a középső pozícióban a hármas kötés a szerkezet a 2-butin mutatja az osztályozás belső alkin.
Így a kapcsolat csak az első és a második szén (1-butin) vagy a második és harmadik szén (2-butin) között lehet. Ennek oka az alkalmazott nómenklatúra, ahol a lehető legkisebb számozás mindig a hármas kötés pozíciójának felel meg.
1-butin
Az 1-butin nevű vegyületet etil-acetilénként is ismert, mivel szerkezetét és négy szénatomjának elrendezését és kötését mutatják. Ha azonban beszélünk butin csak erre a vegyi anyagra hivatkozunk.
Ebben a molekulában a hármas kötés egy terminális szénben található, amely lehetővé teszi a hidrogénatomok rendelkezésre állását, amelyek nagy reaktivitást biztosítanak.
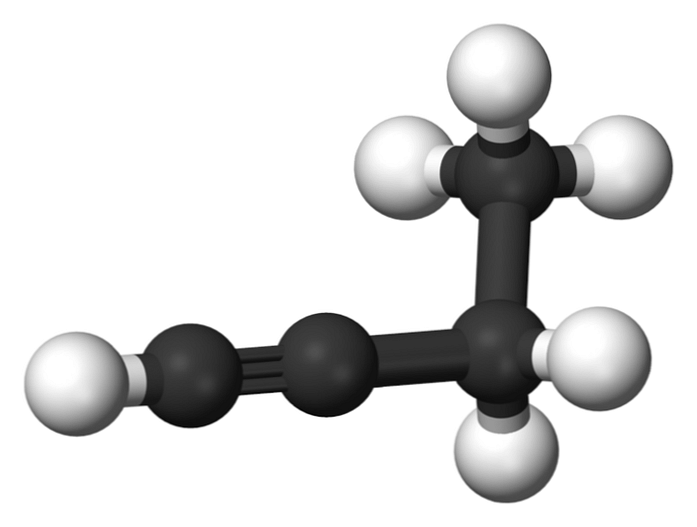
Ez a merev és erősebb kötés, mint a szénatomok közötti egyetlen vagy kettős kötés, stabil 1-butin lineáris geometria konfigurációját biztosítja.
Másrészt, ez a gázhalmazállapotú anyag eléggé tűzveszélyes, így hő jelenlétében könnyen tüzet vagy robbanást okozhat, és levegő vagy víz jelenlétében nagy reaktivitást okozhat..
2-butin
Mivel a belső alkinok nagyobb stabilitást mutatnak, mint a terminális alkinok, lehetővé teszik az 1-butin 2-butinre történő átalakulását.
Ez izomerizációs akkor fordulhat elő melegítésével 1-butin jelenlétében egy bázis (így például nátrium-hidroxid, kálium-hidroxid, NaOCH 3 ...) vagy átültetése 1-butint oldatban kálium-hidroxid (KOH) etanolban (C2H6O).
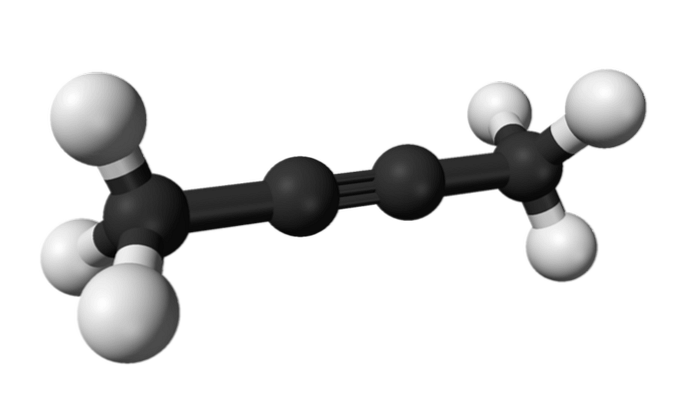
Ugyanígy a 2-butin-ként ismert kémiai vegyületet dimetilacetilénnek (vagy krotonilénnek) is nevezik, amely folyékony és illékony anyagként jelenik meg, amely mesterségesen származik.
A 2-butinben a hármas kötés a molekula közepén van, ami nagyobb stabilitást biztosít, mint az izomerje.
Ezenkívül ez a színtelen vegyület alacsonyabb sűrűségű, mint a víz, bár azt nem oldódik benne, és magas gyúlékonyságú.
tulajdonságok
-A butino szerkezeti képlete (függetlenül attól, hogy melyik izomerre vonatkozik) C4H6, amely lineáris szerkezettel rendelkezik.
-A butin molekula egyik kémiai reakciója az izomerizáció, amelyben a tripla kötés átrendeződése és migrációja következik be a molekulán belül..
-Az 1-Butyne gázfázisban van, nagyon magas gyúlékonysággal és nagyobb sűrűséggel rendelkezik, mint a levegő.
-Ez az anyag is igen reaktív, és hő jelenlétében erőszakos robbanásokat okozhat.
-Továbbá, ha ez a színtelen gáz elégtelen égési reakciót tapasztal, akkor szén-monoxidot (CO) okozhat.
-Ha mindkét izomer magas hőmérsékleten van kitéve, robbanásveszélyes polimerizációs reakciókat tapasztalhatnak.
-A 2-butin folyadékfázisban van, bár a szokásos nyomás- és hőmérsékleti körülmények között is eléggé gyúlékonynak tekinthető.
-Ezek az anyagok erőszakos reakciókat tapasztalhatnak, ha erős oxidáló anyagok jelenlétében vannak.
-Ugyanígy, exoterm reakciók, amelyek következésképpen gáznemű hidrogén felszabadulnak, redukáló fajok jelenlétében jelentkeznek..
-Bizonyos katalizátorokkal (például néhány savas anyaggal) vagy starterrel való érintkezés esetén exoterm típusú polimerizációs reakciók léphetnek fel..
alkalmazások
Mivel különböző tulajdonságokkal rendelkeznek, mindkét izomer különböző felhasználási területei és alkalmazásai lehetnek, az alábbiak szerint:
Először is, az 1-butino egyik alkalmazása gyakran az, hogy a szintetikus eredetű egyéb szerves anyagok előállításának közbenső szakaszaként alkalmazzák..
Másrészről ez a kémiai anyag a gumi és a származékok gyártási iparban használatos; mint például, ha benzolt akar kapni.
Hasonlóképpen, sokféle műanyag termék gyártási folyamatában, valamint sok nagy sűrűségű polietilén anyag gyártásában használják..
Továbbá az 1-butint gyakran használják komponensként egyes fémötvözetek, beleértve az acélt (vasötvözet és szén) vágására és hegesztésére..
Egy másik értelemben, az izomer 2-butint alkalmazunk kombinációban egy másik elemzi alkin propin szintézisében bizonyos anyagok ismert alkilezett hidrokinonok, amikor a folyamat a szintézisét α-Összesen tokoferol (E-vitamin) végezzük.
referenciák
- Wikipedia. (N.d.). Butingázt. A (z) en.wikipedia.org webhelyről származik
- Yoder, C. H., Leber P. A. és Thomsen, M. W. (2010). Szerves kémiai híd: fogalmak és nómenklatúra. A következőt kapta: books.google.co.ve
- Study.com. (N.d.). Butyne: szerkezeti képlet és izomerek. A tanulmányból nyert.
- Pubchem. (N.d.). 1-butint. A pubchem.ncbi.nlm.nih.gov
- Pubchem. (N.d.). 2-butint. A pubchem.ncbi.nlm.nih.gov


