Hidrogén-szulfid (H2S) tulajdonságok, kockázatok és felhasználások
az hidrogén-szulfid a hidrogén-szulfid általános neve (H2S). Hidrazidsavnak tekinthető oldatban (H)2S (aq).
A szulfhidrilsav figyelembe vétele a kémiai vegyület vízben való alacsony oldhatósága ellenére adódik. Szerkezete az 1. ábrán látható (EMBL-EBI, 2005).
Ezért a hidrogén-szulfid vízben kevéssé oldódik. Feloldáskor a sav-szulfidion vagy hidroszulfid képződik (HS-). A hidrogén-szulfid vagy hidrogén-szulfid vizes oldata színtelen, és levegőnek kitéve lassan oxidálja az elemi ként, amely nem oldódik vízben..
Kén-dianion S2- csak erősen lúgos vizes oldatokban létezik; Kivételesen bázikus a pKa> 14 értékkel.
A H2Az S abból ered, hogy az elemi kén érintkezik a szerves anyaggal, különösen magas hőmérsékleten. A hidrogén-szulfid egy kovalens hidrid, amely kémiailag kapcsolódik a vízhez (H2O), mivel az oxigén és a kén ugyanabban a csoportban keletkezik, mint a periodikus táblázat.
Gyakran akkor következik be, ha a baktériumok oxigén hiányában lebontják a szerves anyagokat, például mocsarakban és csatornákban (az anaerob emésztési eljárással együtt). Szintén előfordul vulkáni gázokban, földgázokban és néhány kútvízben.
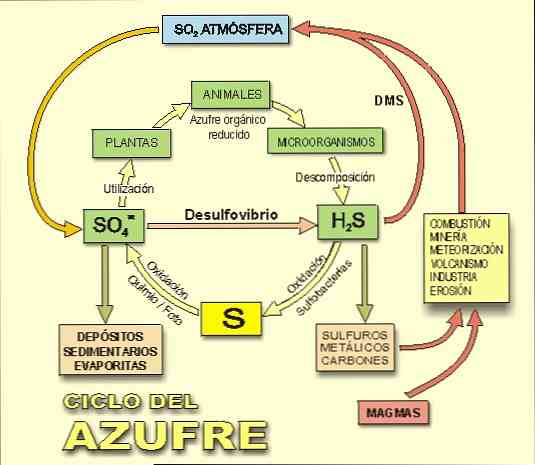
Fontos szem előtt tartani, hogy a hidrogén-szulfid központi szerepet játszik a kénciklusban, a kén biogeokémiai ciklusában a Földön (2. ábra).
Ahogy fentebb említettük, a kén-redukáló és szulfát-redukáló baktériumok oxigén- vagy szerves molekulákból oxidációs energiát termelnek oxigén hiányában a kén- vagy szulfát-hidrogén-szulfid redukálásával.
Más baktériumok hidrogén-szulfidot bocsátanak ki a ként tartalmazó aminosavakból. A baktériumok több csoportja tüzelőanyagként használhat hidrogén-szulfidot, oxidálószerként elemi kénre vagy szulfáttá oxidálva oxigént vagy nitrátot használva..
A tiszta kénbaktériumok és a zöld kénbaktériumok fotoszintézis során hidrogén-szulfidot használnak elektron donorként, így elemi ként képeznek..
Valójában ez a fotoszintézis mód régebbi, mint a cianobaktériumok, az algák és a növények, amelyek elektron-donorként vizet használnak, és oxigént szabadítanak fel (Human Metabolome Database, 2017).
index
- 1 Ahol hidrogén-szulfid keletkezik?
- 2 Fizikai és kémiai tulajdonságok
- 3 Reaktivitás és veszélyek
- 3.1 Belégzés
- 3.2 Bőrrel való érintkezés
- 3.3 Szembe kerülés
- 4 Felhasználások
- 4.1. 1. Kén előállítása
- 4.2 2- Analitikai kémia
- 4.3 - Egyéb felhasználások
Ahol hidrogén-szulfid keletkezik?
Hidrogén-szulfid (H2S) természetesen a nyersolajban, földgázban, vulkáni gázokban és forró forrásokban fordul elő. A szerves anyag bakteriális lebomlását is eredményezheti. Szintén emberi és állati hulladék keletkezik.
A szájban és a bélrendszerben található baktériumok hidrogén-szulfidot termelnek olyan baktériumokból, amelyek növényi vagy állati fehérjéket tartalmazó anyagokat lebontanak.
A hidrogén-szulfid ipari tevékenységből is származhat, mint például élelmiszer-feldolgozás, kokszolókemencék, nátronpapír-gyárak, cserzőüzemek és kőolajfinomítók (Toxikus Anyagok és Betegségek Hivatala, 2011).
Fizikai és kémiai tulajdonságok
A hidrogén-szulfid egy színtelen gáz, amely erős szagú rothadt tojást tartalmaz. A hidrogén-szulfid vizes oldata jellegzetes aroma nélkül színtelen.
A vegyület molekulatömege 34,1 g / mol, a vizes oldat sűrűsége 1,343 g / ml. Olvadáspontja -82 ° C és forráspontja -60 ° C. Vízben enyhén oldódik, 20 ° C-on csak 4 g / liter oldószert képes feloldani (Royal Society of Chemistry, 2015)..
A hidrogén-szulfid savként és redukálószerként reagál. Az oxigén-difluoriddal, bróm-pentafluoriddal, klór-trifluoriddal, diklorid-oxiddal és ezüst-fulmináttal érintkezve felrobban. Rézpor hatására oxigén jelenlétében meggyulladhat és felrobbanhat.
Hasonló módon reagálhat más fémporokkal. Meggyújtja érintkezve fém-oxidok és peroxidok (bárium-peroxid, a króm-trioxid, réz-oxid, ólom-dioxidot, mangán-dioxid, nikkel-oxid, ezüst-oxid, ezüst-dioxid, trioxid tallium, nátrium-peroxid, higany-oxid, kalcium-oxid).
Ezüst-bromát, ólom (II) hipoklorit, réz-kromát, salétromsav, ólom-oxid (IV) és oxid. Meggyulladhat, ha rozsdás vascsöveken halad át. Exotermikusan reagál bázisokkal.
A reakcióhőt nátronmésszel, nátrium-hidroxid, kálium-hidroxid, bárium-hidroxid, ami tüzet okozhat vagy robbanást a reagálatlan részét jelenlétében a levegő / oxigén (hidrogén-szulfid, 2016).
Reaktivitás és veszélyek
A H2Az S-t stabil vegyületnek tekintjük, bár nagyon gyúlékony és rendkívül mérgező.
A vegyület nehezebb, mint a levegő, és jelentős távolságot tud vezetni a gyújtóforráshoz és visszaállítani. Robbanásveszélyes keverékeket képezhet széles levegővel.
Robbanásszerűen reagál bróm-pentafluoriddal, klór-trifluoriddal, nitrogén-trijodiddal, nitrogén-trikloriddal, oxigén-difluoriddal és fenil-diazónium-kloriddal..
Bomlásra felmelegítve rendkívül mérgező kén-oxidok keletkeznek. Nem kompatibilis a sok anyag, beleértve az erős oxidáló szerekkel, fémek, erős salétromsav, bróm-pentafluorid, a klór-trifluoridot, nitrogén-trijodid, triklorid nitrogén, oxigén-difluorid és fenil-diazónium-klorid.
Hidrogén-szulfid (H2S) felelős a munkahelyi mérgező expozíció számos eseményért, különösen az olajiparban. A H klinikai hatásai2Az S koncentrációja és az expozíció időtartama függ.
A H2Az S halálos kimenetelű, ha a koncentráció több mint 500-1000 rész millió (ppm), de az alacsonyabb koncentrációk (pl. 10-500 ppm) expozíciója különböző légúti tüneteket okozhat a rhinitistől az akut légzési elégtelenségig..
A H2Az S több szervre is hatással lehet, ami idegi, szív- és érrendszeri, vese-, máj- és hematológiai rendszerekben ideiglenes vagy tartós rendellenességeket okoz..
A munkahelyi expozíció H esetét mutatja be2S, amely több szerv bevonásához vezet, akut légzési elégtelenség, az akut szepszishez hasonló tüdőgyulladás és sokk megszervezése. Ebben az esetben a beteg enyhe obstruktív és korlátozó tüdőbetegséget és perifériás neuropátiát is kialakított (Al-Tawfiq, 2010).
belélegzés
Belélegzés esetén vegye ki a szabadban, és nyugalmi állapotban tartsa a kényelmes légzést. Ha nem lélegzik, mesterséges lélegeztetést kell adni. Ha a légzés nehéz, a képzett személyzetnek oxigént kell adnia.
Bőrrel való érintkezés
Bőrrel való érintkezés esetén bő vízzel kell mosni. A nyomás alatt álló folyadék fagyást okozhat. Nyomás alatt álló folyadéknak való kitettség esetén a fagyasztási zónát haladéktalanul melegítsük fel meleg 41 ° C-os vízzel.
A víz hőmérsékletének tolerálhatónak kell lennie a normál bőrre. A bőr felmelegedését legalább 15 percig fenn kell tartani, vagy amíg a normál színezés és az érzés vissza nem tér az érintett területre. Masszív expozíció esetén a ruhákat meleg vízzel kell zuhanyozni.
Szembe kerülés
Szembe jutás esetén a szemet alaposan öblítse le vízzel legalább 15 percig. Tartsa nyitva a szemhéjat, és távolítsa el őket a szemgolyóktól, hogy minden felületet alaposan öblítsék.
Lenyelés nem tekinthető lehetséges expozíciós útnak. Minden más esetben azonnal orvoshoz kell fordulni (Praxair, 2016).
alkalmazások
1- Kén előállítása
Egy egység Claus kénkinyerés áll egy tűztér egy hulladékhő kazán, hűtővel kén és számos katalitikus szakaszban, amelyek mindegyike használ újramelegítése, katalizátorágy és kén hűtővel. Jellemzően két vagy három katalitikus lépést alkalmazunk.
A Claus-folyamat a hidrogén-szulfidot elemi kénvé alakítja át egy kétlépéses reakció útján.
Az első lépés a betáplált gáz szabályozott égetését jelenti, hogy a hidrogén-szulfid körülbelül egyharmadát kén-dioxiddá alakítsa át, és a kén-dioxiddal nem égetett hidrogén-szulfid nem katalitikus reakciója.
A második lépésben a Claus-reakció, a hidrogén-szulfid és a kén-dioxid katalizátoron reagál a kén és víz előállítására.
Az égési levegő mennyiségét szorosan szabályozzuk a kén-visszanyerés maximalizálása érdekében, azaz a megfelelő reakciólépés 2: 1-es hidrogén-szulfid reakcióját a kén-dioxidra lefelé irányuló reaktorokon keresztül..
Általában akár 97% -os kén-visszanyerés érhető el (US National Library of Medicine, 2011).
2- Analitikai kémia
Több mint egy évszázadon át a hidrogén-szulfid fontos volt az analitikai kémia területén, a fémionok kvalitatív szervetlen analízisében.
Ezekben az elemzésekben a nehézfém (és nem fém) ionok kicsapódnak (pl. Pb (II), Cu (II), Hg (II), As (III)) az oldatból a H2S expozíció után. A keletkezett csapadék bizonyos szelektivitással ismét feloldódik és így azonosítható.
3 - Egyéb felhasználások
Ezt a vegyületet használják a deuterium-oxid vagy a normál vízből származó nehéz víz elválasztására a Girdler-szulfid-eljárással.
Az Exeteri Egyetem tudósai felfedezték, hogy a sejtek kis mennyiségű hidrogén-szulfid gázzal való kitettsége megakadályozhatja a mitokondriális károsodást.
Amikor a sejtet a betegségben hangsúlyozzák, az enzimeket vonzza a sejtbe, hogy kis mennyiségű hidrogén-szulfidot állítson elő. Ez a tanulmány több következményekkel járhat a stroke, a szívbetegség és az ízületi gyulladás megelőzésében (Stampler, 2014).
A hidrogén-szulfidnak öregedésgátló tulajdonságai lehetnek a sejten belüli destruktív vegyi anyagok blokkolásával, amelyek tulajdonságai hasonlóak a resveratrolhoz, a vörösborban található antioxidánshoz.
referenciák
- A mérgező anyagok és betegségek nyilvántartásának ügynöksége. (2011, március 3.). Hidrogén-szulfid-karbonil-szulfid. Az atsdr.cdc.gov.
- Al-Tawfiq, B. D. (2010). Hidrogén-szulfid expozíció felnőtt férfiban. Annals of Saudi Med. 30 (1) , 76-80.
- EMBL-EBI. (2005, december 13.). hidrogén-szulfid. Az ebi.ac.uk.
- enciklopédia britannica. (S. F.). Hidrogén-szulfid. A britannica.com-ból visszanyert.
- Emberi anyagcsere-adatbázis. (2017. március 2.). Hidrogén-szulfid . A (z) hmdb.ca fájlból származó.
- HIDROGÉNTULÓ. (2016). A cameochemicals.noaa.gov.
- (2016, október 17.). Hidrogén-szulfid biztonsági adatlap. A praxair.com-ról helyreállították.
- Királyi Kémiai Társaság. (2015). Hidrogén-szulfid. A chemspider.com-ból származik.
- Stampler, L. (2014, július 11.). Egy büdös vegyület megvédheti a sejtkárosodást, tanulmányi eredmények. Letöltve az time.com oldalról.
- S. Nemzeti Orvostudományi Könyvtár. (2011, szeptember 22.). Kén, Elemi. A toxnet.nlm.nih.gov.


