Ammónium-hidroxid szerkezet, tulajdonságok, nómenklatúra, felhasználások
az ammónium-hidroxid egy NH molekulaképletû vegyület4OH vagy H5NEM az ammóniagáz (NH) feloldásával nyerhető3) vízben. Ezért kapja meg az ammónia vagy a folyékony ammónia nevét.
Színtelen folyadék, nagyon intenzív és éles szaggal, amely nem szigetelő. Ezek a jellemzők közvetlen kapcsolatban állnak az NH koncentrációjával3 feloldva a vízben; koncentráció, amely valójában gázként egy kis mennyiségű vízben oldott óriási mennyiségű anyagot fedezhet.
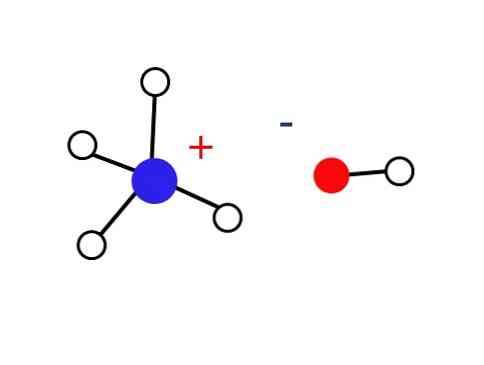
E vizes oldatok jelentősen kis része NH kationokból áll4+ és OH anionok-. Másrészt, nagyon híg oldatokban vagy fagyasztott szilárd anyagokban, nagyon alacsony hőmérsékleten, ammónia található hidrátok formájában, például: NH3∙ H2O, 2NH3∙ H2O és NH3H 2H2O.
Kíváncsi tény, hogy a Jupiter felhőit ammónium-hidroxid hígított oldatai alkotják. A Galileo űrszonda azonban nem találta meg a vizet a bolygó felhőiben, amire az várható, hogy az ammónium-hidroxid képződése ismert; azaz NH-kristályok4OH teljesen vízmentes.
Az ammóniumion (NH4+) a vese tubuláris lumenben az ammónia és a hidrogén egyesülése révén keletkezik, amelyet a vese-tubuláris sejtek választanak ki. Hasonlóképpen, ammónium keletkezik a vese-tubuláris sejtekben a glutamin glutamáttá történő átalakításában, és a glutamát α-ketoglutaráttá történő átalakításában..
Az ammóniát ipari módon a Haber-Bosch módszerrel állítják elő, amelyben a nitrogén- és hidrogéngázok reagálnak; a vas-ion, alumínium-oxid és kálium-oxid katalizátorként történő alkalmazása. A reakciót nagy nyomáson (150 - 300 atmoszféra) és magas hőmérsékleten (400-500 ° C) hajtjuk végre, 10-20% -os hozammal.
A reakcióban ammónia keletkezik, amely oxidálva nitriteket és nitrátokat termel. Ezek elengedhetetlenek a salétromsav és a műtrágyák, például az ammónium-nitrát előállításához.
index
- 1 Kémiai szerkezet
- 1.1 Ammónia jég
- 2 Fizikai és kémiai tulajdonságok
- 2.1 Molekuláris képlet
- 2.2 Molekulatömeg
- 2.3 Megjelenés
- 2.4 Koncentráció
- 2.5 Szag
- 2.6 Íz
- 2.7 Küszöbérték
- 2.8 Forráspont
- 2.9 Oldhatóság
- 2.10 Oldhatóság vízben
- 2.11 Sűrűség
- 2.12 Gőzsűrűség
- 2.13 Gőznyomás
- 2.14 Maró hatás
- 2,15 pH
- 2.16 Disszociációs állandó
- 3 Nómenklatúra
- 4 Oldhatóság
- 5 Kockázatok
- 5.1 Reaktivitás
- 6 Felhasználások
- 6.1 Élelmiszerben
- 6.2 Gyógyszerek
- 6.3 Ipari és egyéb
- 6.4 A mezőgazdaságban
- 7 Referenciák
Kémiai szerkezet
Amint azt a meghatározás jelzi, az ammónium-hidroxid ammóniagáz vizes oldatából áll. Ezért a folyadékon belül nincs meghatározva az NH-ionok véletlen elrendezésétől eltérő szerkezet4+ és OH- vízmolekulák által szolvatált.
Az ammónium- és hidroxil-ionok az ammónia hidrolízisének egyensúlyi termékei, ezért gyakori, hogy ezek az oldatok szúrós szaggal rendelkeznek:
NH3(g) + H2O (l) <=> NH4+(ac) + OH-(AQ)
A kémiai egyenlet szerint a vízkoncentráció nagy csökkenése az egyensúlyt több ammónia képződéséhez vezetne; azaz az ammónium-hidroxid melegítésével ammóniagőzök szabadulnak fel.
Ezért az NH ionok4+ és OH- nem tudnak kristályt képezni a földi körülmények között, ami olyan következményekkel jár, mint amilyen az NH szilárd bázis4OH nem létezik.
Ezt a szilárd anyagot csak az elektrosztatikusan kölcsönhatásban lévő ionokból kell készíteni (a képen látható)..
Ammóniás jég
Azonban 0 ° C alatti hőmérsékleten, és óriási nyomásokkal körülvéve, például a jeges holdak magjában, az ammónia és a víz fagyasztásában. Ezáltal szilárd keverékben kristályosodnak, változatos sztöchiometriai arányokkal, a legegyszerűbb NH3∙ H2O: ammónia-monohidrát.
Az NH3∙ H2O és az NH3H 2H2Vagy ezek ammóniás jég, mert a szilárd anyag a vízmolekulák és a hidrogénkötések által összekapcsolt ammónia kristályos elrendezéséből áll.
A T és P változását figyelembe véve, az összes fizikai változót szimuláló számítási vizsgálatok és ezekre a jégre gyakorolt hatásuk alapján egy NH fázis átmenetre kerül sor3∙ nH2Vagy egy NH fázisra4OH.
Ezért csak ezekben az extrém körülmények között, az NH4Az OH lehet a jégen belüli protonáció terméke az NH között3 és a H2O:
NH3(s) + H2O (s) <=> NH4OH (ok)
Megjegyezzük, hogy ezúttal az ammónia hidrolízisével ellentétben az érintett fajok szilárd fázisban vannak. Ammónia jég, amely sóvá válik ammónia felszabadítása nélkül.
Fizikai és kémiai tulajdonságok
Molekuláris képlet
NH4OH vagy H5NO
Molekulatömeg
35,046 g / mol
megjelenés
Színtelen folyadék.
koncentráció
Legfeljebb 30% (NH ionok esetén)4+ és OH-).
szag
Nagyon erős és éles.
aroma
acre.
Küszöbérték
34 ppm nem specifikus detektáláshoz.
Forráspont
38 ° C (25%).
oldhatóság
Csak vizes oldatban létezik.
Oldhatóság vízben
Korlátlan arányban keverhető.
sűrűség
0,90 g / cm33 25 ° C-on.
Gőzsűrűség
Az egységként vett levegőhöz viszonyítva: 0.6. Vagyis kevésbé sűrű, mint a levegő. Logikusan azonban a jelentett érték ammóniát jelent gázként, nem pedig vizes oldataira vagy NH-ra4OH.
Gőznyomás
2,60 mmHg 25 ° C-on.
Maró hatás
Képes feloldani a cinket és a rézet.
pH
11,6 (1 N oldat); 11,1 (0,1 oldat N) és 10,6 (0,01 N oldat).
A disszociációs állandó
pKb = 4,767; Kb = 1,71 x 10-5 20 ° C-on
pKb = 4,751; Kb = 1,774 x 10-5 25 ° C-on.
A hőmérséklet emelkedése szinte észrevétlenül emelkedik az ammónium-hidroxid bázisosságára.
nómenklatúra
Melyek az NH általános és hivatalos nevei?4OH? Az IUPAC által megállapítottak szerint annak neve ammónium-hidroxid, mivel a hidroxil-anionot tartalmazza.
Az ammónium terhelése +1 egyértékű, miért használják a nómenklatúrát. A készlet nevét: ammónium-hidroxid (I).
Bár az ammónium-hidroxid kifejezés alkalmazása technikailag hibás, mivel a vegyület nem izolálható (legalábbis nem a Földön, amint azt az első részben részletesen ismertettük).
Emellett az ammónium-hidroxid az ammónia és a folyékony ammónia nevét kapja.
oldhatóság
Az NH4OH, mivel a szárazföldi körülmények között nincs só, nem becsülhető meg, hogy az oldható-e különböző oldószerekben.
Azonban elvárható, hogy ez vízben rendkívül oldható legyen, mivel oldódása óriási mennyiségű NH-t szabadít fel3. Elméletileg csodálatos mód lenne az ammónia tárolására és szállítására.
Más oldószerekben, amelyek képesek hidrogénkötéseket elfogadni, mint amilyenek az alkoholok és aminok, elvárható, hogy ez is nagyon jól oldódik benne. Itt az NH kation4+ hidrogénhidak és az OH- úgy működik, mint mindkettő.
Az ilyen kölcsönhatások a metanollal például a következők: H3N+-H - OHCH3 és HO- - HOCH3 (OHCH3 azt jelzi, hogy az oxigén a hidrogénkötést kapja, nem azt, hogy a metilcsoport H-hez kapcsolódik..
kockázatok
-Szembe kerülve irritációt okozhat, amely szemkárosodáshoz vezethet.
-Maró hatású. Ezért a bőrrel érintkezve irritációt okozhat, és a reagens nagy koncentrációjában bőrégést okozhat. Az ammónium-hidroxidnak a bőrrel való ismételt érintkezése szárazságát, viszketését és bőrpírját (dermatitist) okozhat..
-Az ammónium-hidroxid-permet belélegzése a légutak akut irritációját okozhatja, melyet fulladás, köhögés vagy légszomj jellemez. Az anyag hosszantartó vagy ismételt expozíciója visszatérő bronchiás fertőzést okozhat. Emellett az ammónium-hidroxid belélegzése irritálhatja a tüdőt.
-Az ammónium-hidroxid nagy koncentrációjának kitettsége orvosi vészhelyzet lehet, mivel a tüdőben felgyülemlő folyadék (tüdőödéma) előfordulhat..
-A 25 ppm koncentrációt egy 8 órás munkamenetben expozíciós határértéknek tekintették olyan környezetben, ahol a munkavállaló az ammónium-hidroxid káros hatásának van kitéve..
reakcióképesség
-Emellett az ammónium-hidroxid-expozícióval járó potenciális egészségkárosodás egyéb olyan óvintézkedéseket is figyelembe kell venni, amelyeket az anyaggal való munka során figyelembe kell venni.
-Az ammónium-hidroxid számos fémzel reagálhat, például: ezüst, réz, ólom és cink. Ez is reagál ezeknek a fémeknek a sóival, hogy robbanásveszélyes vegyületeket képezzen és hidrogéngázt szabadítson fel; amely viszont gyúlékony és robbanásveszélyes.
-Hevesen reagálhat erős savakkal, például sósavval, kénsavval és salétromsavval. Hasonlóképpen, ugyanúgy reagál a dimetil-szulfáttal és a halogénekkel.
-Reagál erős bázisokkal, például nátrium-hidroxiddal és kálium-hidroxiddal, gáznemű ammónia előállítására. Ez ellenőrizhető, ha az oldat egyensúlyi állapota megfigyelhető, amelyben az OH ionok hozzáadódnak- az egyensúlyt NH-képződésbe helyezi3.
-A réz és az alumínium fémek, valamint más horganyzott fémek nem használhatók fel ammónium-hidroxid kezelésére, mivel ezek rázó hatással vannak rájuk..
alkalmazások
Az ételben
-Sok élelmiszerben adalékanyagként használják, amelyben a táplálékfelület ropogós, pH-szabályozó és befejező szereként működik..
-Az ammónium-hidroxidot tartalmazó élelmiszerek listája kiterjedt, és magában foglalja a sült termékeket, sajtokat, csokoládét, cukorkákat és pudingokat..
-Az ammónium-hidroxidot az FDA az élelmiszer feldolgozásához biztonságos anyagnak minősíti, feltéve, hogy a megállapított szabványokat betartják.
-A húskészítményekben antimikrobiális szerként alkalmazzák, így képes eltávolítani az olyan baktériumokat, mint az E. coli, csökkentve a kimutathatatlan szintre. A baktériumok megtalálhatók a szarvasmarha bélében, alkalmazkodva a savas környezethez. Az ammónium-hidroxid a pH szabályozásával gátolja a bakteriális növekedést.
gyógyászati
-Az ammónium-hidroxidnak több terápiás alkalmazása van, beleértve:
-A 10% -os oldatot légzési reflex stimulánsként használják
-Külsőleg a bőrön rovarcsípések és harapások kezelésére használják. - Az emésztőrendszerre antacid és karminatív hatású, azaz segít a gázok eltávolításában..
Ezen túlmenően, akut és krónikus izom-csontrendszeri fájdalmak helyi kezelésére használják. Az ammónium-hidroxid hatásos hatása következtében a véráramlás, a bőrpír és az irritáció helyi növekedése következik be..
Ipari és egyéb
-A NOx csökkentésére (erősen reaktív gázok, mint például a nitrogén-oxid (NO) és a nitrogén-dioxid (NO2)) a kéménykibocsátás és a kéménykibocsátás NOx-csökkentése.
-Ezt lágyítószerként használják; Festékek adalékanyagai és felületek kezelésére.
-Ez növeli a haj porozitását, lehetővé téve a foltok pigmentjeinek nagyobb behatolását, ami jobb felületet eredményez.
-Az ammónium-hidroxidot antimikrobiális szerként használják a szennyvíz kezelésében. Emellett beavatkozik a klór-amin szintézisébe. Ez az anyag a medencevíz tisztításakor a klórhoz hasonló funkciót tölt be, amelynek előnye, hogy kevésbé mérgező.
-Korróziógátló szerként használják az olajfinomítás során.
-Tisztítószerként használják különböző ipari és kereskedelmi termékekben, több felületen használva, beleértve: rozsdamentes acél, porcelán, üveg és sütő.
-Ezenkívül mosószerek, szappanok, gyógyszerek és tinták gyártására is használják.
A mezőgazdaságban
Bár az ammónium-hidroxid nem közvetlenül műtrágyaként adható be, ezt a funkciót teljesíti. Az ammóniát a légköri nitrogénből Haber-Bosch módszerrel állítják elő, és a forráspontja alatt (-33 ° C) hűtve szállítják a felhasználási helyekre..
A nyomás alatt álló ammóniát gőz formájában befecskendezik a talajba, ahol azonnal reagál az edafikus vízzel, és áthalad az ammónium-formába (NH4+), amely a talaj kationcserélő helyén marad. Emellett ammónium-hidroxid keletkezik. Ezek a vegyületek nitrogénforrást jelentenek.
A foszfort és a káliumot együtt a nitrogén a növekedéshez nélkülözhetetlen növények fő tápanyagainak hármasa.
referenciák
- Ganong, W. F. (2002). 19. kiadás. Szerkesztői Modern kézikönyv.
- A. D. Fortes, J. P. Brodholt, I. G. Wood és L. Vocadlo. (2001). Az ammónia-monohidrát (NH.) \ T3∙ H2O) és ammónium-hidroxid (NH4OH). Amerikai Fizikai Intézet. J. Chem. Phys., 115, 15, 15.
- Helmenstine, Anne Marie, Ph.D. (2017. február 6.). Ammónium-hidroxid tények. A lap eredeti címe: thinkco.com
- Pochteca Group. (2015). Ammónium-hidroxid. pochteca.com.mx
- NJ Egészség (N.d.). A veszélyes anyagokról szóló adatlap: ammónium-hidroxid. [PDF]. A lap eredeti címe: nj.gov
- Kémia tanuló. (2018). Ammónium-hidroxid. A lap eredeti címe: chemistrylearner.com
- Pubchem. (2018). Ammónium-hidroxid. Lap forrása: pubchem.ncbi.nlm.nih.gov


