Kalcium-hidroxid formula, tulajdonságok, reaktivitás és felhasználások
az kalcium-hidroxid, hidratált mészként vagy hígított mészként is ismert (Ca) általános képletű szervetlen vegyület.2.
A kalcium-hidroxid a fémhidroxidokhoz hasonlóan polimer szerkezetet alkalmaz, amely megegyezik a magnézium-hidroxid (Mg (OH) )éval.2) brucita néven is ismert.
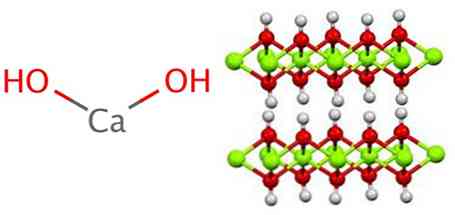
Látható, hogy ebben a szerkezetben hidrogénhidak képződnek. A kalcium-hidroxidot ipari úton szintetizáljuk, kalcium-oxidot, más néven mészet vagy mészhéjat, vízzel reagáltatva a következő reakció szerint:
CaOH + H2O → Ca (OH)2
A laboratóriumban a vizes kalcium-klorid és nátrium-hidroxid közötti reakcióval is előállítható.
A kalcium-hidroxid természetesen fordul elő, de ritkán ásványi formájában, mint portlandit, amely néhány vulkáni és metamorf kőzetben található. (Kalcium-hidroxid-képlet - kalcium-hidroxid felhasználás, tulajdonságok, szerkezet és képlet, 2005-2017).
Ez a vegyület a cement, az oldószer és az ipari tisztítószerek (például építési termékek), a padlószalagok, a téglatisztítók, a cement-sűrítő termékek és sok más termék számára is elérhető..
A vizes oldatot rendszerint limewaternek nevezik. A mészvizet úgy állítjuk elő, hogy a kalcium-hidroxidot tiszta vízben keverjük és a Ca (OH) feleslegét szűrjük.2 nem oldódott fel.
Ha a mészvízhez felesleges kalcium-hidroxidot adagolunk, kalcium-hidroxid-részecskék szuszpenzióját kapjuk, amely tejszerű megjelenést eredményez, amely esetben a mésztej közös neve. A mész tejének vagy a mész (telített víz) telített oldatának pH-ja 12,3, ami alapvető jellegű.
A kalcium-hidroxid fizikai és kémiai tulajdonságai
A kalcium-hidroxid fehér vagy színtelen por, szagmentes. A vizes oldatban (telített oldatokban) a feloldatlan kalcium-hidroxid felülúszója miatt tejszerű megjelenést mutat.
A telítetlen oldatok általában tiszta és színtelen oldatok, enyhe földes szaggal és keserű, kálium-hidroxid-ízzel. A vegyület megjelenését a 3. ábra mutatja be (Royal Society of Chemistry, 2015)..

A kalcium-hidroxid molekulatömege 74,093 g / mol, sűrűsége 2,211 g / cm3 szilárd állapotban. Olvadáspontja 580 ° C. Gyengén oldódik vízben, így 1,89 gramm / liter 0 ° C-on, 1,73 g / l 20 ° C-on és 0,66 g / l 100 ° C-on feloldható..
Glicerinben és savas oldatokban oldódik. Alkoholban oldhatatlan (Nemzeti Biotechnológiai Információs Központ, S.F.).
A kalcium-hidroxid részlegesen vízben oldódik, így olyan oldatot hozunk létre, amely mérsékelt bázis. Lime víz vagy Ca (OH)2 (aq) Reagál savakkal sók képződésére és bizonyos fémek, például alumínium támadására. A mészvíz könnyen reagál a szén-dioxiddal, hogy kalcium-karbonátot képezzen.
Ca (OH)2 + CO2 → CaCO3 + H2O
A nitroparafinok, nitrometán, nitropropán stb. Szervetlen bázisokkal, például kalcium-hidroxiddal sókat képeznek. Ezek a száraz sók robbanásveszélyesek. A vegyület kémiailag hasonló a nátrium-hidroxidhoz (NaOH) vagy nátrium-oxidhoz (Na2O). Ezek a savakat exotermikusan semlegesítik, sók és víz képződnek.
Ezeknek az anyagoknak a vízzel való összekeverése veszélyes hőmennyiséget eredményezhet, mivel az alap feloldódik vagy hígul. A bázisok bizonyos fémekkel (például alumíniummal és cinkkel) reagálnak, hogy fém-oxidokat vagy hidroxidokat képezzenek, és hidrogéngázt képezzenek.
A bázisok polimerizációs reakciókat indíthatnak polimerizálható szerves vegyületekben, különösen epoxidokban. Tűzveszélyes és / vagy mérgező gázok keletkezhetnek ammóniumsókkal, nitridekkel, halogénezett szerves anyagokkal, különböző fémekkel, peroxidokkal és hidroperoxidokkal. Ez a fajta vegyület gyakran katalizátorként szolgál (kémiai adatlap CALCIUM HYDROXIDE, S.F.).
Reaktivitás és veszélyek

A kalcium-hidroxid egy stabil vegyület, bár nem kompatibilis az erős savakkal. Ez irritáló vegyületnek minősül, és a veszélyek között kiemelhető:
Maró hatású a szemre (szaruhártya-károsodást vagy vakságot okoz) és a bőrt (gyulladást és hólyagokat termelnek).
A por belélegzése irritációt okoz a gyomor-bélrendszerben vagy a légzőrendszerben, amelyet égés, tüsszögés és köhögés jellemez. A súlyos túlzott expozíció tüdőkárosodást, aszfxiát, eszméletvesztést vagy halált okozhat. A szemgyulladást vörösség, irritáció és viszketés jellemzi (anyagbiztonsági adatlap, kalcium-hidroxid, 2013).
A szemek ismételt expozíciója alacsony porszint esetén irritációt és helyi bőrpusztulást vagy bőrbőrgyulladást okozhat a bőrön. A por ismételt belélegzése változó fokú légúti irritációt vagy tüdőkárosodást okozhat.
Ha ez a vegyi anyag érintkezik a szemmel, azonnal nagy mennyiségű vízzel kell mosni, esetenként felemelve az alsó és a felső szemhéjakat. Azonnal orvoshoz kell fordulni. A kontaktlencséket nem szabad használni a vegyszerrel végzett munka során.
Ha ez a vegyi anyag érintkezik a bőrrel, a szappannal és vízzel szennyezett bőrt azonnal le kell öblíteni. Ha ez a vegyi anyag behatol a ruházatba, azonnal vegye ki a ruhát és öblítse le a bőrt vízzel. Ha a mosás után az irritáció továbbra is fennáll, forduljon orvoshoz.
Ha ezt a vegyszert nagy mennyiségben belélegzik, a kitett személyt azonnal friss levegőre kell vinni. Ha a légzés leállt, hajtsa végre a szájról a szájba újraélesztést, és az áldozatot melegen és pihenés közben is tartsa. Azonnal forduljon orvoshoz.
Lenyelés esetén azonnal orvoshoz kell fordulni, és ha lehetséges, tartályt vagy címkét kell mutatni (kalcium-hidroxid mérgezés, 2017).
Kezelés és tárolás
- A vegyületet száraz tartályban kell tartani.
- Ne lélegezze be a port.
- A terméket soha nem szabad hozzáadni ehhez a termékhez.
- A szellőzés hiánya esetén hozzon megfelelő légzőkészüléket.
- Kerülje a bőrrel és szemmel való érintkezést.
- Tartsa távol a savaktól.
- Tartsa szorosan zárva a tartályt.
- A tartályt hűvös és jól szellőző helyen kell tartani. Legfeljebb 25 ° C-on tárolandó.
Felhasználások és alkalmazások

A kalcium-hidroxid nagy mennyiségben keletkezik, könnyen kezelhető és általában olcsó, ezért számos jelentős felhasználás és alkalmazás létezik.
A kalcium-hidroxid jelentős alkalmazása olyan, mint a flokkulálószer a vízben és a szennyvízben. Pelyhes, töltött szilárd anyagot képez, amely segít a kisebb részecskék eltávolításában a vízből, ami könnyebb terméket eredményez.
Ezt az alkalmazást a kalcium-hidroxid alacsony költsége és alacsony toxicitása teszi lehetővé. Édesvíz kezelésére is használják a víz pH-jának növelése érdekében. A cél az, hogy a csövek ne korrodálódjanak, ha az alapvíz savas.
Egy másik nagyszerű alkalmazás a papíriparban, ahol nátrium-hidroxid előállítására használják. Ez a konverzió az ismert kraft folyamat egyik komponense, amelyet a cellulóz extrakciójában használnak.
Az élethordozó rendszerekben, mint például a szén-dioxid-mosógépben, különösen zárt áramkörű búvár-re-légzőkészülékekben, ahol a lítium-hidroxid, ami több maró hatású, túl kockázatosnak tekinthető.
A fehérítés és vakolás összetevőjeként használják az úgynevezett mészhabarcsokkal. Az útépítésben a kalcium-hidroxid a talaj minőségének javítására szolgál.
A Nemzeti Egészségügyi Intézetek szerint a fogászati munkában a kalcium-hidroxidot általában antimikrobiális szerként használják, és a választott anyag védőréteget képez, melyet apikális gátnak neveznek..
Az apikális korlátokat általában a pulpális nekrózis elkerülésére használják olyan helyzetekben, amikor az endodontikus műtét különösen nehéz lenne, ami általában az éretlen állandó fogak eredménye..
Mivel a kalcium-hidroxid segíthet fertőtleníteni egy fogat, ahol a fertőzés már létezik, rövid távú kezelésként alkalmazható a fájdalom és a gyulladás csökkentésére az endodontikus műtét előkészítése során (Gottfried Schmalz, 2009).
A tengervíz adalékanyagaként szolgál, mivel csökkenti a légköri CO2-t és csökkenti az üvegházhatást.
A fémek előállítása során a mészet a hulladékgázáramba injektálják a savak, például a fluoridok és kloridok semlegesítésére, mielőtt a légkörbe engednék.
Néhány haj relaxációs termékben aktív kalcium-hidroxidot alkalmazunk.
A Cornell Center for Materials Research szerint a kalcium-hidroxid kiegyenesítheti a göndör hajat, mert megszakítja a ciszteineket összekötő diszulfidkötéseket, a magasabb koncentrációban jelen lévő aminosavakat természetes göndör hajban. Ezen kötések megszakítása és kalcium-hidroxiddal való lezárása véglegesen megváltoztatja a kezelt haj fizikai szerkezetét.
A Bordeaux-keverékben a kalcium-hidroxid semlegesíti az oldatot, és tartós fungicidet képez.
Az olajfinomító iparban olaj adalékanyagok (szalicilátok, szulfátok, fenolok), petrolkémiai iparban történő gyártására használják a különböző márkák szilárd olajának előállítására, valamint a kémiai iparban a kalcium-sztearát előállítására. . Általában a szén-dioxid és a gáz felszívódásának vizsgálatára használják.
A kalcium-hidroxidot a fékbetétek gyártásához használják, száraz keverékek előállítására festéshez és díszítéshez, valamint a peszticidek keverékeinek gyártásához..
Kálcium-kiegészítőként és pH / karbonát pufferként is használják a zátony akváriumok korallos akvakultúrájában.
Ez egy „alternatív” természetes rovarölő, a legtöbb a mászó rovarok meghal kapcsolatba vele, beleértve a kullancsokat, bolhák, bogarak és lárvák (Russiver, 2015).
A kalcium-hidroxid hatékony megoldás a haj szétválasztására az állatok bőréből, előkészítve a bőr előállítására.
A kalcium-hidroxid és a meleg víz keveréke olyan fürdőt hoz létre, amelyben a friss bőreket négy napig áztatni kell, és gyakran meg kell rázni. Ez a folyamat lazítja a hajat és a bőrt, olyan mértékben, hogy általában kézzel eltávolítható.
Alacsony toxicitása és alapvető tulajdonságainak lágysága miatt az oltott mész széles körben használatos az élelmiszeriparban, hogy:
- A cukorrépa vagy a cukorrépa nyers gyümölcslé tisztázása a cukoriparban, az alkoholtartalmú italok és üdítőitalok, a savanyúságok és más élelmiszerek feldolgozási vize..
- Készítse el a kukorica tortillákat (segítsen a kukoricamagnak összeállni). A mészzel főzött kukorica nixtamálvá alakul, ami jelentősen növeli a niacin biohasznosulását, ízletesebb és könnyebben emészthető..
- Tisztítsuk meg a kalcium- és magnézium-karbonát-sóoldatot az élelmiszer- és gyógyszerészeti felhasználásra szánt só előállításához.
- A gyümölcsitalok, például a narancslé, és a csecsemőkészítmények megerősítése (BAUM, 2013).
referenciák
- BAUM, J. (2013, augusztus 16.). Kalcium-hidroxid felhasználás. A livestrong.com-tól: livestrong.com.
- Kalcium-hidroxid-képlet - kalcium-hidroxid felhasználás, tulajdonságok, szerkezet és képlet. (2005-2017). A (z) softschools.com webhelyről származik.
- Kalcium-hidroxid mérgezés. (2017. február 7.). A medlineplus.gov.
- Kémiai adatlap CALCIUM HYDROXIDE. (S. F.). A cameochemicals.noaa.gov.
- Gottfried Schmalz, D. A. (2009). A fogászati anyagok biokompatibilitása. Berlin: springer.
- Anyagbiztonsági adatlap Kalcium-hidroxid. (2013, május 21.). A sciencelab-ből származik: sciencelab.com.
- Nemzeti Biotechnológiai Információs Központ. (S. F.). PubChem összetett adatbázis; CID = 6093208. A pubchem.ncbi.nlm.nih.gov.
- Királyi Kémiai Társaság. (2015). Kalcium-hidroxid. A ChemSpider-ből származik: chemspider.com.
- Russiver, M. (2015, augusztus 17.). Mi a kalcium-hidroxid? A quora-ból származik: quora.com.


