Jellemző apoláris molekulák, hogyan azonosíthatók és példák
az apoláris molekulák azok azok, amelyek a struktúrájukban elektronjuk szimmetrikus eloszlását mutatják be. Ez akkor lehetséges, ha atomjainak elektronegativitása kicsi, vagy ha az elektronegatív atomok vagy csoportok megszakítják hatásukat a molekulában.
Nem mindig "abszolút" abszolút. Emiatt a poláris polaritású molekulákat néha apolárisnak tekintik; Ez azt jelenti, hogy a dipoláris momentuma μ közel van a 0-hoz. Itt belép a relatív terepébe: milyen alacsonynak kell lennie μ-nak, ha egy molekulát vagy vegyületet tekintünk apolárisnak?
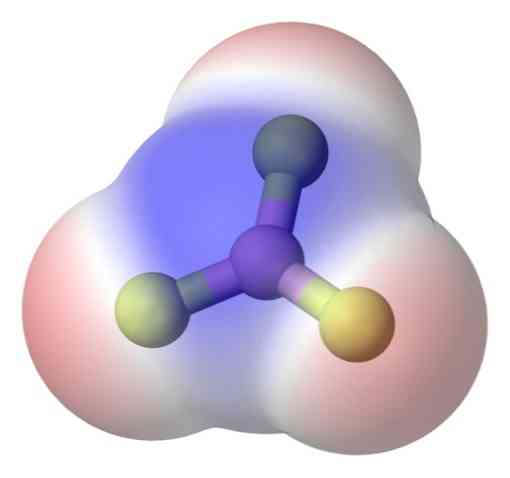
Ahhoz, hogy jobban kezeljék a problémát, a bór-trifluorid-molekula, a BF3 (felső kép).
A fluoratom sokkal elektronegatívabb, mint a bóratom, és ezért a B-F kötések polárisak. Azonban a BF molekula3 szimmetrikus (trigonális sík) és magában foglalja a három B-F pillanat vektor törlését.
Ily módon apoláris molekulák is keletkeznek, még a poláris kötések meglétével is. A generált polaritás kiegyensúlyozható egy másik poláris összeköttetés létezésével, amely ugyanolyan nagyságrendű, mint az előző, de az ellenkező irányba orientált; ahogy a BF-ben történik3.
index
- 1 Az apoláris molekula jellemzői
- 1.1 Szimmetria
- 1.2 Elektronegativitás
- 1.3 Intermolekuláris erők
- 2 Hogyan lehet azonosítani őket?
- 3 Példák
- 3.1 Nemesgázok
- 3.2 Diatóma molekulák
- 3.3 Szénhidrogének
- 3.4 Egyéb
- 4 Referenciák
Az apoláris molekula jellemzői
szimmetria
Ahhoz, hogy a poláris kötések hatásai egymásnak megszűnjenek, a molekulának meghatározott geometriai szerkezettel kell rendelkeznie; például lineáris, az első látásra a legegyszerűbb.
Ez a szén-dioxid (CO2), amely két poláris kapcsolattal rendelkezik (O = C = O). Ez annak a ténynek köszönhető, hogy a C = O összeköttetések két dipoláris pillanata egymás felé fordul, és a második a másik felé, 180 ° -os szögben..
Ezért az egyik első tulajdonság, amelyet egy molekula "apolaritásának" madárszemként történő értékelése során figyelembe kell venni, az, hogy megfigyeljük, milyen szimmetrikus ez..
Tegyük fel, hogy a CO helyett2 a COS-molekula (O = C = S), karbonil-szulfid.
Most már nem apoláris molekula, mivel a kén elektronegativitása kisebb, mint az oxigén; és ezért a C = S dipól momentum különbözik a C = O-tól. Ennek eredményeképpen a COS egy poláris molekula (hogyan poláros a liszt egy másik zsákból).
Az alsó kép grafikusan összefoglalja mindazt, amit éppen most leírtak:
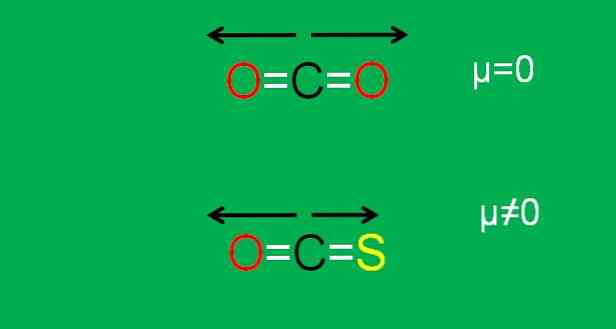
Megjegyezzük, hogy a C = S kötés dipólusszáma kisebb, mint a C = O kötés a COS molekulában.
elektronegativitási
A Pauling-skála elektronegativitása 0,65 (a francium esetében) és a 4,0 (a fluor) értékei között van. Általában a halogének nagy elektronegativitással rendelkeznek.
Amikor a kovalens kötést alkotó elemek elektronegativitásának különbsége kisebb vagy egyenlő, mint 0,4, azt mondják, hogy apoláris vagy nem poláris. Az egyetlen olyan molekula, amely valóban apoláris, az azonos atomok (például hidrogén, H-H) közötti kapcsolatok által alkotott molekulák..
Intermolekuláris erők
Ahhoz, hogy egy anyag vízben oldódjon, elektrosztatikusan kölcsönhatásba kell lépnie a molekulákkal; az apoláris molekulák nem képesek kölcsönhatásba lépni.
Az apoláris molekulákban az elektromos töltések nem korlátozódnak a molekula egyik végére, hanem szimmetrikusan (vagy homogénen) eloszlanak. Ezért nem képes kölcsönhatásba lépni a dipol-dipólus erőkön.
Ezzel szemben az apoláris molekulák kölcsönhatásba lépnek egymással a londoni diszperziós erőkön keresztül; ezek azonnali dipolok, amelyek polarizálják a szomszédos molekulák atomjainak elektronikus felhőjét. Itt a molekulatömeg a molekulák fizikai tulajdonságaiban meghatározó tényező.
Hogyan lehet azonosítani őket?
-Talán az egyik legjobb módja az apoláris molekula azonosításának az a különböző poláros oldószerekben való oldhatósága, amelyek általában rosszul oldódnak benne..
-Általában az apoláris molekulák természetükben gázhalmazállapotúak. Ezek is vízzel nem elegyedő folyadékokat képezhetnek.
-Az apoláris szilárd anyagokat lágyak jellemzik.
-A diszperziós erők, amelyek együtt tartják őket, általában gyenge. Emiatt az olvadási vagy forráspontjaik alacsonyabbak, mint a poláris jellegű vegyületeké.
-Az apoláris molekulák, különösen a folyékony formában, a villamos energia szegény vezetői, mivel nem rendelkeznek nettó elektromos töltéssel.
Példák
Nemesgázok
Bár nem molekulák, nemesgázok tekinthetők apolárnak. Feltételezve, hogy két rövid ideig két atomja kölcsönhatásba lép, He-He, ez az interakció molekulaként tekinthető (félig); molekula, amely a természetben apoláris lenne.
Diatomiás molekulák
Diatóma molekulák, például H2, Br2, az I2, Cl2, az O2, és az F2, ezek apolárisak. Ezek általános képlettel rendelkeznek2, A-A.
szénhidrogének
Mi van, ha A atomok csoportja? Más apoláris vegyületek előtt lenne; például etán, CH3-CH3, amelynek szénváza lineáris, C-C.
Metán, CH4, és etán, C2H6, ezek apoláris molekulák. A szén-dioxid 2,55-ös elektronegativitással rendelkezik; míg a hidrogén elektronegativitása 2,2. Ezért van egy alacsony intenzitású dipol vektor, amely hidrogéntől szénig terjed.
De a metán és az etán molekulák geometriai szimmetriája miatt a molekulákban a dipol vektorok vagy a dipol pillanatok összege nulla, így a molekulákon nincs nettó töltés.
Általában ugyanez történik az összes szénhidrogén esetében, és még akkor is, ha ezekben telítetlenek (kettős és hármas kötések), az apoláris vagy alacsony polaritású vegyületeknek tekinthetők. Hasonlóképpen, a ciklikus szénhidrogének apoláris molekulák, mint például a ciklohexán vagy a ciklobután..
mások
A szén-dioxid molekulái (CO2) és szén-diszulfid (CS)2) apoláris molekulák, mindkettő lineáris geometriájú.
A szén-diszulfidban a szén elektronregativitása 2,55, míg a kén elektronegativitása 2,58; úgy, hogy mindkét elemnek gyakorlatilag azonos elektronegativitása van. Nincs dipol vektor generálása, ezért a nettó töltés nulla.
A következő CCl molekulák is vannak4 és AlBr3, mindkét apolár:
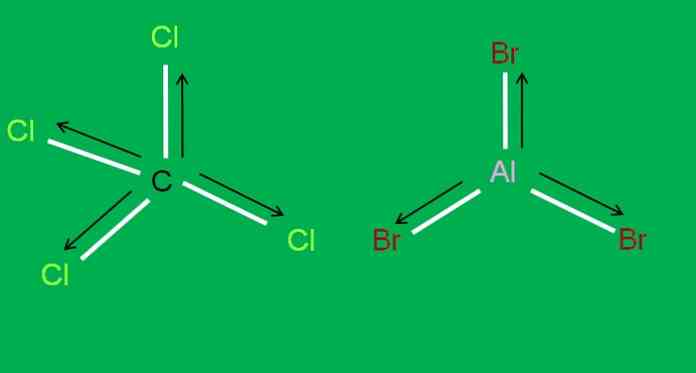
Az alumínium-tribromidban az AlBr3 ugyanaz, mint a BF-ben3, a cikk elején. Eközben a szén-tetraklorid esetében a CCl4, a geometria tetraéderes és szimmetrikus, mivel minden C-Cl kapcsolat egyenlő.
Hasonlóképpen, a CX általános képletű molekulák4 (CF4, CI4 és CBr4), szintén apolárisak.
És végül, egy apoláris molekula akár nyolcadik, de a kén-hexafluorid, az SF esetében is lehet.6. Valójában bármilyen geometriája vagy szerkezete lehet, amennyiben szimmetrikus és elektronikus eloszlása homogén.
referenciák
- Carey F. A. (2008). Szerves kémia Karbonsavak. (Hatodik kiadás). Mc Graw-hegy.
- Cedrón J., Landa V., Robles J. (2011). A molekulák polaritása. A lap eredeti címe: corinto.pucp.edu.pe
- Tutor Vista. (2018). Nempoláris molekula. Lap forrása: chemistry.tutorvista.com
- Helmenstine, Anne Marie, Ph.D. (2019. január 28.). Példák a poláris és nem poláris molekulákra. A lap eredeti címe: thinkco.com
- Kurtus R. (2016. szeptember 19.). Poláris és nem poláris molekulák. Bajnokok iskolája. A lap eredeti címe: school-for-champions.com
- Ganong W. (2004). Orvosi fiziológia 19. kiadásth. A Modern kézikönyv szerkesztősége.


