Lítium-oxid formula, tulajdonságok, kockázatok és felhasználások
az lítium-oxid egy (Li) általános képletű szervetlen kémiai vegyület2Vagy a kis lítium-peroxiddal együtt képződik, amikor a lítiumfém levegőben égetik és oxigénnel kombinálják.
Az 1990-es évekig a fém- és lítiumpiacot az ásványi lerakódásokból származó amerikai termelés dominálta, de a XXI. Század elején a legtöbb termelés nem amerikai forrásból származott; Ausztrália, Chile és Portugália volt a világ legfontosabb szállítója. Bolívia a lítium lerakódások fele a világon, de nem nagy termelő.
A legfontosabb kereskedelmi forma a lítium-karbonát, Li2CO3, az ásványi anyagokból vagy sóoldatokból több különböző eljárással.
Amikor a lítiumot égetik a levegőben, a fő termék a Li-oxid fehér oxidja2Ezenkívül néhány lítium-peroxid keletkezik, Li2O2, fehér is.
A lítium-hidroxid, LiOH vagy lítium-peroxid, Li2O2 termikus bomlása révén is elvégezhető.
4Li (s) + O2(g) → 2Li2O (s)
2LiOH (ok) + hő → Li2O (s) + H2O (g)
2Li2O2+ hő + → 2Li2O (s) + O2(G)
Fizikai és kémiai tulajdonságok
A lítium-oxid olyan fehér szilárd anyag, amelyet lítiának neveznek, és nincs aromája és sós íze. Megjelenése a 2. ábrán látható (Nemzeti Biotechnológiai Információs Központ, 2017).

2. ábra: lítium-oxid megjelenése
A lítium-oxid olyan kristályok, amelyek antiflorit-geometriájúak, mint a nátrium-kloridé (a kocka középen az arcokon). Kristályszerkezete a 3. ábrán látható (Mark Winter [Sheffield Egyetem és WebElements Ltd, 2016].
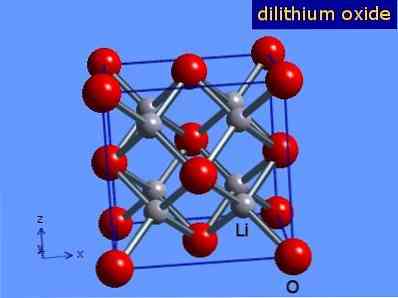
3. ábra: a lítium-oxid kristályos szerkezete.
Molekulatömege 29,88 g / mol, sűrűsége 2,013 g / ml, az olvadási és forráspontok 1438 ° C és 2066 ° C. A vegyület vízben, alkoholban, éterben, piridinben és nitrobenzolban nagyon jól oldódik (Royal Society of Chemistry, 2015).
A lítium-oxid könnyen reagál a vízgőzzel, így hidroxidot képez, és szén-dioxiddal karbonátot képez; ezért tiszta és száraz légkörben kell tárolni és kezelni.
Az oxid-vegyületek nem vezetnek villamos energiához. Azonban a perovskit bizonyos strukturált oxidjai olyan elektromos vezetőképességűek, amelyek a szilárd oxid tüzelőanyag-cellák és az oxigéntermelő rendszerek katódjában alkalmazhatók..
Ezek olyan vegyületek, amelyek legalább egy oxigén-anionot és egy fémkationot tartalmaznak (American Elements, S.F.)..
Reaktivitás és veszélyek
A lítium-oxid stabil vegyület, amely összeegyeztethetetlen az erős savakkal, a vízzel és a szén-dioxiddal. Tudomásunk szerint a lítium-oxid kémiai, fizikai és toxikológiai tulajdonságait nem vizsgálták és nem jelentették be mélyrehatóan.
A lítiumvegyületek toxicitása a vízben való oldhatóságuk függvénye. A lítiumion központi idegrendszeri toxicitással rendelkezik. A vegyület erősen maró hatású, ha belélegezve vagy lenyelve érintkezik a szemmel, a bőrrel (ESPI METALS, 1993).
Szembe kerülés esetén ellenőrizze, hogy kontaktlencséket visel-e, és azonnal távolítsa el őket. A szemet legalább 15 percig le kell öblíteni folyó vízzel, miközben a szemhéjak nyitva maradnak. Használhat hideg vizet. A kenőcs nem használható a szem számára.
Ha a vegyi anyag érintkezik a ruházattal, távolítsa el azt a lehető leggyorsabban, védve a saját kezeit és testét. Helyezze az áldozatot biztonsági zuhany alatt.
Ha a kémia felhalmozódik az áldozat kitett bőrére, például a kezekre, óvatosan és óvatosan mossa le a folyóvízzel és a nem koptató szappannal szennyezett bőrt. Használhat hideg vizet. Ha az irritáció továbbra is fennáll, forduljon orvoshoz. A szennyezett ruhát újrafelhasználás előtt mossuk.
Belélegzés esetén az áldozatot jól szellőztetett helyen kell hagyni. Ha az inhaláció súlyos, az áldozatot a lehető leghamarabb ki kell üríteni egy biztonságos területre.
Lazítsa meg a feszes ruhákat, például ing gallér, övek vagy nyakkendő. Ha az áldozatnak nehéz lélegezni, oxigént kell beadni. Ha az áldozat nem lélegzik, a szájról szájra történő újraélesztés történik.
Mindig vegye figyelembe, hogy veszélyes lehet a segítséget nyújtó személy számára a szájról szájra történő újraélesztéshez, ha a belélegzett anyag mérgező, fertőző vagy maró hatású.
Minden esetben azonnal forduljon orvoshoz (SIGMA-ALDRICH, 2010).
alkalmazások
Lítium-oxidot használnak kerámia mázak fluxusaként, és kék rézzel és rózsákkal, kobalttal. A lítium-oxid vízzel és gőzzel reagál, lítium-hidroxid képződik, és el kell különíteni őket.
Lítium-oxid (Li2O) magas trícium-potenciáljával vonzó DT-fúziós erőmű tenyésztőanyagának vonzó jelöltje a lítium-atomok nagy sűrűsége miatt (a többi lítium- vagy fémes lítium-kerámiához képest) és vezetőképessége miatt. viszonylag magas termikus (LITIUM OXIDE (Li2O), SF).
Li2Vagy magas hőmérsékletnek van kitéve neutron besugárzás alatt a fúziós takarók működése során. Ilyen körülmények között nagyszámú besugárzási hiba lép fel Li-ben2Vagy mint például a hélium által kiváltott duzzanat, viszonylag magas termikus expanzió, szemcsés növekedés, LiOH (T) képződés és alacsony hőmérsékleten történő kicsapódás és LiOH (T) tömegének magas hőmérsékleten történő szállítása.
Ezen kívül a Li2Vagy a feszültségek a Li hőtágulása közötti különbségek miatt lesznek2O és szerkezeti anyagok. Ezek Li jellemzői2Vagy kihívást jelentő mérnöki problémákhoz vezetnek a takaró gyártásában és tervezésében.
Lehetséges új felhasználás a kobalt és a lítium-oxid helyettesítése katódként a lítium-ion akkumulátorokban, amelyeket a mobiltelefonoktól a laptopokig, valamint az akkumulátorral működtetett autókhoz használnak (Reade International Corp, 2016).
referenciák
- Mark Winter [A Sheffieldi Egyetem és a WebElements Kft. (2016). webelements. Lítiumból: dilithium oxide webelements.com.
- Amerikai elemek. (S. F.). Lítium-oxid. Az americanelements americanelements.com-ról származik.
- ESPI METALS. (1993, június). Lítium-oxid. Készült az espimetals.com-ról.
- LITIUMOXID (Li2O). (S. F.). A ferp.ucsd.edu ferp.ucsd.edu.
- Nemzeti Biotechnológiai Információs Központ. (2017. június 24.). PubChem összetett adatbázis; CID = 166630. A PubChem pubchem.ncbi.nlm.nih.gov.
- Reade International Corp. (2016). Lítium-oxid por (Li2O). A reade.com-ról
- Királyi Kémiai Társaság. (2015). Lítium-oxid.A chemspiderchemspider.com webhelyről.
- Sigma-Aldrich. (2010). Anyagbiztonsági adatlap Lítium-oxid. A chemblink chemblink.com-ból készült.


