Mangán-oxid (MnO2) kémiai szerkezete, tulajdonságai és felhasználásai
az mangán-oxid (MnO2) egy szervetlen kémiai vegyület, amelyet a mangán elem +4 oxidációs szám és oxigén képez, amely oxidok képződése során oxidációs száma -2. A mangán (IV) -oxid és a mangán-anhidrid neve is ismert.
Ez egy szilárd, sötét és fekete kávé között. Természetesen mint ásványi piroluszit, fekete és kristályosodott dendritek (elágazó nyúlások). Az etilén és a kálium-permanganát reakciójában a kálium-permanganát oxidáló hatásának köszönhetően fekete maradékként nyerhető..

Az oxidálószer jellegéből adódóan nagyon fontos az üvegiparban, mivel kiküszöböli a vasvegyületekből származó zöld színt és átalakítja azt vasból..
index
- 1 Kémiai szerkezet
- 2 Tulajdonságok
- 3 Használat
- 3.1 Katalizátorként
- 4 Az egészségre gyakorolt hatások
- 5 Referenciák
Kémiai szerkezet
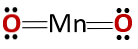
A vegyület kémiai szerkezete megfelel az anhidridé, és nem a bázikus oxidok szerkezetének, ahogyan azt várták, mert egy fémből és nem fémből áll..
Ez a különleges eset a mangán által a különböző oxidációs állapotokban feltételezett viselkedésnek köszönhető. Így az oxidációs állapotokhoz a +2 és +3 az MnO és az Mn oxidokat képezi2O3 illetve a vízzel való reakció során a mangán-hidroxidot és a mangán-hidroxidot képezik.
Azonban az Mn2O3 enyhén savas közegben úgy viselkedik, mint egy anhidrid. Az oxidációs állapot +4, +6 és +7, az MnO2, a MnO3 és a MnO4 a vízzel reagáltatva savakat képeznek.
Egy enyhén savas közegben a MnO2 úgy viselkedik, mint egy bázikus oxid, így képezheti a megfelelő hidroxidot.
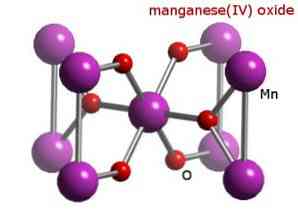

Emlékeztetni kell arra, hogy ebben az esetben nincs említés az amfoter tulajdonságokról, amelyek szerint a vegyület savként vagy bázisként viselkedhet. Ez az Mn viselkedésének különleges esete.
tulajdonságok
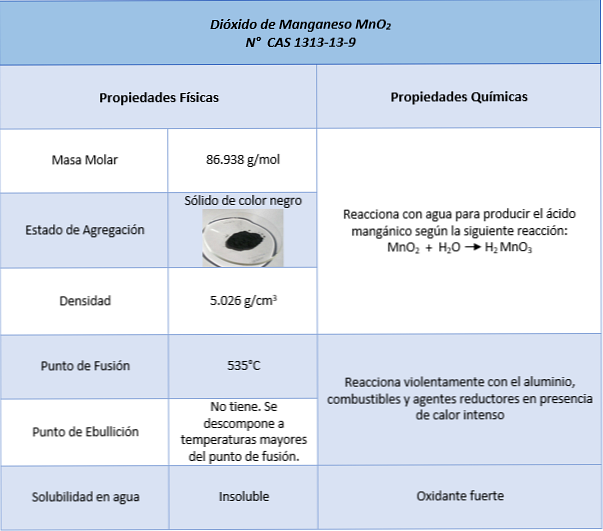
alkalmazások
- Ezt mangánforrásként használják
- Az alkáli elemek oxidálószerként
- Üveg, kerámia és porcelán festékek.
- A klór és a jód előállításához.
- A hidrogén-peroxid bomlásakor a gáz halmazállapotú oxigén és víz képződéséhez.
- A kálium-klorát bomlási reakciójában gáz-halmazállapotú oxigén és kálium-klorid előállítására.
- Acetonban vagy diklór-metánban oldva, a primer alkoholokat aldehiddé oxidáljuk, és a ketonok másodlagosvá válnak..
- Alkáli elemek gyártása.
Katalizátorként
Ez vonatkozik az oxid-redukciós reakciókra, a szulfidok, például H eltávolítására2S és kationok, mint a Fe+2 és Mn+2 , az ilyen típusú vegyületekkel szennyezett, a felszín alatti vizekben található arzén és rádió.
Ez a szennyeződés akár mérgező anyagok ellenőrizetlen dömpingjével, a szennyezett talaj mosásával, akár kémiai elemek jelenlétével állítható elő a vízkivételkor..
A MnO2 A szűrőként használt piroluszitból nyert nagy tisztaság (Filox) a leghatékonyabb eszköz ennek a osztálynak a felszín alatti vízből való eltávolítására..
Az egészségre gyakorolt hatások
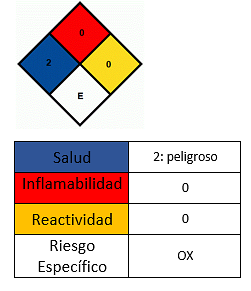
- Kerülje a bőrrel való érintkezést.
- Érintkezés esetén mossa le a megfelelő területet.
- Ne lélegezze be a porokat.
- A szemkontaktusnál az irritáció és a bőrpír látható. Bő vízzel le kell mosni, hagyja, hogy a víz átmegy a szemen, és súlyos orvosi segítséget kérjen.
- A bőrrel érintkezve irritáció és vörösség figyelhető meg. Az érintett területet bő vízzel és szappannal mossuk.
- A tartós bőrkontaktus eltávolítja a természetes zsírt, ami dermatitist vált ki.
- A belégzés influenzaszerű állapotot okozhat (fémes füstök). Az állapotot magas láz, hidegrázás, szájszárazság és torok, izomfájdalom és fejfájás jellemzi.
- Ez irritálja a légutakat és növelheti a légúti fertőzések (tüdőgyulladás) előfordulását. A szervetlen mangán-sók tüdőkön keresztül történő felszívódásával történő mérgezés nem valószínű, de krónikus mérgezés léphet fel..
- A mangán-dioxid hosszú ideig tartó porra vagy füstjére való krónikus expozíció befolyásolhatja a központi idegrendszert, és a Parkinson-kór, a járási nehézségek, az izomgörcsök és a viselkedési változások kialakulásához vezethet..
- Lenyelés hasi fájdalmat és hányingert okozhat.
- Nem gyúlékony, de segít a tüzet az izzólámpákban elterjedni. 535 ° C feletti hőmérsékletre melegítve az anyag mangán-oxidra (III) Mn2O3 és oxigén, amely gyúlékony és fokozza a tűzveszélyt. Ebben az esetben a tüzet hab vagy széndioxiddal kell eloltani.
- Kiömlés esetén a személyi védelem nélkül ne kezelje a vegyületet.
- Tárolja a vegyületet szorosan lezárt tartályokban, hideg és száraz helyen, és távolítsa el az inkompatibilis anyagokat, például szerves anyagot és éghető anyagot..
- A tárolóhelynek száraznak kell lennie, és a padlónak ellenállónak kell lennie a savas korrózióval és jó vízelvezetéssel..
- Személyes védőfelszerelést kell használni, például kesztyűt, védőszemüveget, gőzellenes szűrőmaszkot, port és füstöt.
referenciák
- B, (2015), Mangán-dioxid, The Royal Society of Chemistry - Kémia világ, kémiai világból.
- Karal, (2014), Mangneso-dioxid, Biztonsági adatlap, Visszanyerés, karal.com.mx
- A virtuális tanár (2015/02/25). Mangán szervetlen vegyületek (1. különleges eset) - elméleti lecke), a youtube.com
- Ecured, (s.f), mangán-dioxid, visszanyert az ecured.cu-tól
- Angarita G, Johnny., (2017), Mangán-dioxid: Kivételes technológia. Hidroteco, visszaállt a hydrotecocr.com webhelyről
- Fernández, G., (2015), MnO mangán-dioxid2/ aceton, Szerves kémia, A quimicaorganica.net-ből visszanyert
- Tronox, (2011), mangán-dioxid, biztonsági adatlap, helyreállított, tronox.com


