Gramfolt alapok, anyagok, technika és felhasználás
az Gram folt A diagnosztikai mikrobiológia legegyszerűbb és leghasznosabb festési technikája. Ezt a technikát a dán orvos, Hans Christian Gram 1884-ben hozta létre, aki a sejtfal összetételének megfelelően sikerült besorolni a baktériumokat Gram-pozitív és Gram-negatív értékben..
A technika Hucker 1921-ben bizonyos módosításokat hajtott végre a reagensek stabilizálása és a folt minőségének javítása érdekében, így a Gram-festék Gram-Hucker néven is ismert..
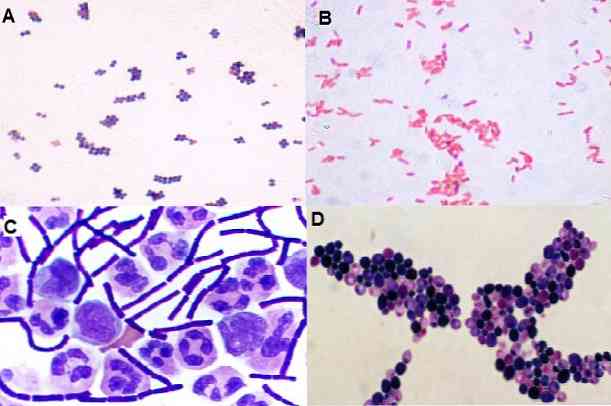
Ezzel a módszerrel megfigyelhető a mikroorganizmusok formája is, azaz, hogy ezek kókuszok, bacillák, kokcobacillák, pleomorf, szálasak. Az űrben való eloszlása mellett: klaszterben, láncban, izoláltan, párban, tetrádban stb..
Bakteriális fertőzés gyanúja esetén a beérkezett minták többségét egy dián kell elosztani, és a mikroszkóp alatt vizsgálni kell Grammal..
A Gram jelentése az orvosnak tájékoztatja, hogy a mikroorganizmus milyen típusú lehet a fertőzés oka, mielőtt a termés végeredményét megszerzi.
Bizonyos esetekben a beteg élete nagyon veszélyeztetett, így az orvosoknak sürgősen szükségük van a Gram-jelentésre, hogy empirikus kezelést nyújtsanak, miközben várják a mikroorganizmus azonosítását..
Például, ha a Gram kiderül, hogy a cerebrospinális folyadékban Gram-pozitív kókuszok vannak, az orvos a kezdeti terápiát az antibiotikumokkal, amelyek az ilyen típusú baktériumokat kiküszöbölik, az erre vonatkozó protokolloknak megfelelően..
Amint a végeredmény az elkülönített mikroorganizmus nevével és annak megfelelő antibiotikumával érkezik, az orvos megvizsgálja, hogy módosítsa-e a terápiát. Ezt a döntést a mikroorganizmus érzékenységének tanulmányozása alapján fogják meghozni, és azt, hogy a mikroorganizmus milyen antibiotikumokkal rendelkezik, és a beteg fejlődését..
index
- 1 Alapítvány
- 2 Anyagok
- 3 Festékek és reagensek készítése
- 3.1 Kristály lila oldat
- 3.2 Iodo-Lugol
- 3.3 Fehérítés
- 3.4 Kontraszt
- 4 A reagensek tárolása
- 5 A színezendő minta terjedésének előkészítése
- 5.1 -A közvetlen minták grammja
- 5.2. A növények grammja
- 6 Technika
- 7 Segédprogram
- 8 Gyakori hibák
- 9 Referenciák
alapítvány
Ez egy olyan módszer, amely 4 alapvető lépést tesz lehetővé: festés, rögzítés a szennyeződéssel, elszíneződés és összehúzódás. Ezért ez a technika a baktériumok színezésén túl megkülönbözteti őket.
A kristály ibolya az első színezőanyag. Affinitása van a peptidoglikánra és a lila színez minden baktériumot, majd elhelyezi a pisztolyt, ami káros hatású, vagyis oldhatatlan kristály violet-jód - ribonukleáris fehérjék képződését idézi elő a sejten belül.
Gram-pozitív baktériumok, amelyek peptidoglikán vastag falával rendelkeznek, több komplexet képeznek (kristály violet-jód), ezért megtartják a festéket.
Azt is befolyásolja, hogy a Gram-pozitív baktériumok fala nagyobb mennyiségű telítetlen savat tartalmaz, amely nagy affinitást mutat az oxidálószerekkel szemben (Lugol).
Eközben a Gram-negatív baktériumoknak vékony réteg peptidoglikánja van, ami a baktériumokat kevésbé bonyolítja, mint a Gram-pozitív baktériumok..
Ezután jön az elszíneződés lépése, ahol a Gram-pozitív és a Gram-negatív baktériumok másképp viselkednek.
A gram-negatív baktériumok olyan külső membránt tartalmaznak, amely gazdag lipopoliszacharidokban, amely a sejtfal része. A zsírokat alkohol acetonnal érintkezve elpusztítják, így a külső membrán destabilizálódik, a lila kristály felszabadul.
Ily módon a színt a piros színnel szafraninnal vagy alapfukszinnal ellensúlyozzák.
Gram-pozitív baktériumok esetében ellenállnak az elszíneződésnek, mivel a fehérítő hatással van a pórusok bezárására, ami megakadályozza a kristály violet / jódkomplex kilépését.
Ezért az ibolyakristály színezése stabil, és nincs helye szafraninnak vagy fukszinnak. Emiatt ezek a baktériumok intenzív kék vagy lila foltokat festenek.
anyagok
A Gram színező készlet a következőket tartalmazza:
- Lila kristály
- Lugol
- Aceton-alkohol
- Safranin vagy alapvető fukszin
Festékek és reagensek készítése
Kristály lila oldat
A megoldás:
Lila kristály -2 gr
95% -20 ° C etil-alkohol
B megoldás:
Ammónium-oxalát -0,8 g
Desztillált víz-80 cm3
A lila kristály végső előállításához az 1:10 oldatot desztillált vízzel kell hígítani, és 4 rész B-oldattal elegyíteni. A keveréket felhasználás előtt 24 órán át tárolni kell. A szűrőt egy lombikban szűrjük, amint borostyánfestés történik egy papírszűrő segítségével.
A naponta felhasználandó mennyiség cseppentővel borostyán üvegbe kerül.
Jód-Lugol
Mérjük meg és mérjük meg az egyes vegyületek jelzett mennyiségét az alábbiak szerint:
Iodo kristályai - 1gr
Kálium-jodid - 2gr
Desztillált víz -300 cm3
A kálium-jodid kis mértékben feloldódik a vízben, majd hozzáadjuk a jódot. Az oldatot borostyánsárga színű palackba borítjuk.
A naponta felhasználandó mennyiséget cseppentővel egy kisebb borostyán üvegbe visszük át.
fehérítés
95% etil-alkohol -50 ml
Aceton - 50 ml
Ez egyenlő részekben készül. Fedjük le jól, hajlamos elpárologni.
Helyezzen egy üvegbe cseppentővel.
Ez a készítmény mérsékelt idővel 5-10 másodpercig változik, és a leginkább ajánlott.
A kezdők inkább 95% -os etil-alkoholt használnak, ahol az elszíneződés 10 és 30 másodperc között lassabb.
Míg a legtapasztaltabbak tiszta acetont használnak, ahol az elszíneződés nagyon gyorsan 1-5 másodpercig történik.
kontraszt
Safranin törzsoldat
Safranina -2,5 gr
Etil-alkohol 95% -100 cm3
A megadott mennyiségű safranint 100 ml etil-alkoholban oldjuk 95% -ra..
A működő szafranin oldatot az alapoldatból állítjuk elő.
Ehhez mérjünk fel 10 cm3 törzsoldatot, adjunk hozzá 90 cm3 desztillált vizet a 100 ml elkészítéséhez.
Javasoljuk, hogy a naponta használt mennyiséget cseppentővel töltse a borostyán üvegbe.
Gram-negatív Gram-Hucker foltokkal, például bizonyos anaerobokkal festett mikroorganizmusok, Legionella sp, Campylobacter sp és Brucella sp, sokkal jobban festhetők, ha a Kopeloff által a Gram-Hucker festéshez, a Gram-Kopeloff-féle festéshez készített módosítást alkalmazzuk.
Ez a technika megváltoztatja a safranin festéket alapfukszinnal. Ezzel a módosítással lehetséges a fent említett mikroorganizmusok hatékony színezése.
A reagensek tárolása
Az elkészített színezékeket szobahőmérsékleten kell tárolni.
A minta előkészítése színre terjedt
A mintának legalább 105 mikroorganizmusok előfordulása előtt a mikroorganizmus megfigyelését valószínűsíti. A direkt mintákból vagy szilárd vagy folyékony közegekből lehet terjeszteni.
A terjesztéseknek egységesnek, jól elosztottnak és nem túl vastagnak kell lenniük a jelenlévő struktúrák jobb megjelenítéséhez.
-A közvetlen minták grammja
Vizelet gramm centrifuga nélkül
A vizeletet összekeverjük és 10 μl-t helyezünk egy csúszdára. A legalább egy baktérium / Immersion mező megfigyelése azt jelzi, hogy fertőzés van.
Ez azt jelenti, hogy a tenyészet körülbelül 100 000 CFU / ml-nél (105 CFU / ml) az esetek 85% -ában.
Ez a módszer nem hasznos 100 000 CFU-nál alacsonyabb telepek számában.
LCR Gram
A CSF-et centrifugálni kell, a felülúszót eltávolítani kell, és a pelletet egy csúszdán el kell helyezni. Ez a folyadék normál körülmények között steril; a baktériumok megfigyelése fertőzést jelez.
Gramm légzési minták
A Gram, a hörgő vagy a bronchoalveoláris öblítés, bár sokféle mikroorganizmus létezik, mindig a diagnózisban fog vezetni, ráadásul hasznos a megfigyelt sejtek típusa is..
A köpet esetében a kenetet a minta legtisztább részével kell elkészíteni.
Stool Gram
Nem ajánlott Gram-ot végrehajtani az ilyen típusú mintákra, mivel nincs diagnosztikai értéke.
-Gramos növények
Ezeket kétféleképpen lehet elvégezni: az egyik a folyékony növényekből, a másik a szilárd növényekből.
Folyékony növények
A folyékony tenyészetekből rendkívül egyszerű; az öngyújtó alatt a zavaros tápközeg több pörköltjét veszik fel, és egy tiszta és száraz csúszdára helyezik, amely körkörös mozdulatokat tesz lehetővé a központtól a periféria felé, hogy az anyagot egyenletesen terjesszék.
Megengedhető, hogy spontán megszáradjon a levegőben. Szárítás után az anyagot hőre rögzítik. Ehhez egy 3 szorító segítségével a 3 lapot a Bunsen-égő lángján 4-szer áthúzzuk, ügyelve arra, hogy az anyagot ne égesse el..
A lapot hagyjuk lehűlni és a színhídra helyezni.
Szilárd növények
A Gram-foltok szilárd kultúrából történő kiterjesztésének végrehajtásához tegye a következőket:
Mielőtt kiválasztanánk a befogadandó telepeket, elő kell készíteni a csúszkát, két csepp hozzávetőlegesen steril fiziológiás sóoldatot.
Ha az eredeti tenyésztőlemez többféle kolóniát tartalmaz, akkor mindegyikből izolált kolónia kerül kiválasztásra a Gram végrehajtására. Mindegyik kolóniát a platina hurokkal fogjuk fel, hogy feloldjuk azt a sóoldatban előzetesen elhelyezett sóoldatban.
A középponttól a perifériához körkörös mozdulatokat adunk, hogy a kolónia homogénen eloszlik a diara..
Megengedhető, hogy spontán megszáradjon a levegőben. Szárítás után a lapot hővel rögzítjük, a fentiekben leírtak szerint (a csúszka lángja az öngyújtóval), ügyelve arra, hogy ne égesse az anyagot.
Ezt az eljárást minden egyes kolóniával kell elvégezni. Egy papírlapon meg kell jegyezni a megfigyelt sorrendet, például:
1. kolónia: Sárga béta-hemolitikus kolónia: Gram-pozitív kokszokat figyeltünk meg klaszterekben
2. kolónia: krém kolónia, hemolízis nélkül: Gram-negatív kokcobacillákat figyeltünk meg.
Minden lapot fel kell címkézni, hogy tudjuk, mit figyelünk.
technika
A Gram festési technika rendkívül egyszerű és viszonylag olcsó, és nem hagyható ki egy mikrobiológiai laboratóriumban.
Ugyanez történik a következőképpen:
- Rögzítse a kenetet hővel és helyezze a színes hídon.
- A lapot 1 percig teljesen lila üveggel fedjük le.
- Mossuk le vízzel. Ne száradjon
- Fedjük le a lemezt Lugol-oldattal, hagyjuk 1 percig. Mossuk le vízzel. Ne száradjon.
- A keveréket 5-10 másodpercig keverjük, enyhe keverés közben aceton-alkoholban. Vagy tegye a lapot függőleges helyzetbe, és cseppentesse a cseppentőszert a felületre, amíg a megmaradt lila üveg el nem húzódik. Ne lépje túl.
- Mossuk le vízzel. Ne száradjon.
- Helyezze vissza a lapot a színes hídra, és fedezze 30 másodpercig safraninnal (Gram-Hucker) vagy 1 perccel alapfukszinnal (Gram-Kopeloff)..
- Mossuk le vízzel
- Hagyja, hogy függőleges levegőben spontán száradjon.
Szárítás után helyezzünk egy csepp merülőolajat, hogy az optikai mikroszkópban 100X-os célt vegyük figyelembe.
hasznosság
Ez a technika lehetővé teszi, hogy megkülönböztessük a legtöbb baktérium morfotípusos különbségeit.
Az élesztők is ezt a színt különböztetik meg. Elveszik a kristály ibolyát, azaz Gram-pozitívak.
Másrészt megkülönböztethetőek a Gram-pozitív spóraképző bacillák, amelyekben a bacilluson belül tiszta tér van, ahol az endospórus kialakult, bár a spórák nem foltosak jól. A spórák használatához más technikákat, például a Shaeffer-Fultont használnak.
Meg kell jegyezni, hogy ez a folt nem szolgál minden típusú baktérium színezésére, vagyis vannak olyan esetek, amikor a festés nem működik.
Ebben az esetben említhetők a sejtfal hiányzó baktériumok. Például: Mycoplasma nemzetség, szferoplasztok, Ureaplasma, L-formák és protoplasztok.
Szintén rosszul baktériumok, amelyek mikolsavakban gazdag falakkal rendelkeznek, mint például a Mycobacteriumok és az intracelluláris baktériumok, mint például a Chlamydias és a Rickettsias..
A legtöbb spirochetális baktérium foltja is nem hatékony.
Vannak ugyanazon nemzetségbe tartozó baktériumok, amelyek ugyanabban a mintában megfigyelhetők, mint a Gram-pozitív és a Gram-negatív. Ha ez megtörténik, akkor változó Gram-foltnak nevezzük, amely a tápanyagok, a hőmérséklet, a pH-érték vagy az elektrolitkoncentráció változásából adódik..
Gyakori hibák
Túlzottan fehérítse
Az elszíneződési lépésben való túlzás a hamis gram-negatív mikroorganizmusok megfigyelését okozhatja.
Ne várjon elegendő száradási időt a merülő olaj hozzáadásához:
Ez a hiba zsíros micellák kialakulását okozza, amelyek megnehezítik a jelenlévő struktúrák megfigyelését. Ez akkor történik, amikor az olaj csatlakozik a kenetben lévő vízmolekulákhoz.
Fordítsa vissza a reagensek sorrendjét:
Egy ilyen hiba miatt a Gram-negatív baktériumok lila, azaz hamis Gram-pozitívak lesznek.
Használjon régi növényeket (szilárd vagy folyékony):
Gram-pozitív baktériumokat okozhat Gram-negatívnak (hamis Gram-negatív). Ez azért van, mert a régi kultúrákban valószínű, hogy halott vagy romlott baktériumok vannak, és ezekben a körülmények között a baktériumok nem tartják meg a lila kristályt.
Használjon nagyon régi Lugol-oldatot:
Idővel elveszíti tulajdonságait és a színe elhalványul. Ha a már degenerált reagenst használjuk, akkor nem fogja jól megkötni a kristály violetet, ezért lehetőség van a mikroorganizmusok vizuális megjelenítésére..
Kék háttér
A megfelelően elszíneződött háttér piros lesz. A kék háttér azt jelzi, hogy az elszíneződés elégtelen.
referenciák
- Ryan KJ, Ray C. 2010. Sherris. mikrobiológia Orvosi, 6. kiadás McGraw-Hill, New York, USA
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobiológiai diagnózis. (5. kiadás). Argentína, szerkesztő Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Bailey & Scott mikrobiológiai diagnózisa. 12 ed. Argentínában. Panamericana S.A szerkesztő
- Casas-Rincón G. 1994. General Mycology. 2. kiadás Universidad Central de Venezuela, Könyvtár kiadások. Venezuela, Caracas.
- "Gram folt" Wikipédia, A szabad enciklopédia. Okt. 4, 2018, 23:40 UTC. 2018. december 9., 17:11. Készült az es.wikipedia.org oldalról.
- González M, González N. 2011. Orvosi mikrobiológiai kézikönyv. 2. kiadás, Venezuela: A Carabobo Egyetem média- és kiadványigazgatósága.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Alapvető festés a mikrobiológiai laboratóriumban. A fogyatékossággal kapcsolatos kutatás. 2014 3 (1): 10-18.


