Trypanosoma brucei jellemzői, morfológiája, biológiai ciklusa, tünetei
Trypanosoma brucei Ez egy extracelluláris parazita protozoa. A Kinetoplastidae osztályba, a Trypanosomatidae családba tartozó családba tartozik Trypanosoma. Két alfaj, amelyek két különböző változatot idéznek elő az afrikai humán trippanoszomiasisban, vagy "alvási betegségnek" is nevezik..
Trypanosoma brucei subsp. gambiense, a nyugati és közép-szubszaharai Afrikában található esetek krónikus formáját és 98% -át okozza. Trypanosoma brucei subsp. rhodesience a szubszaharai Afrika központjában és keleti részén található akut forma oka.
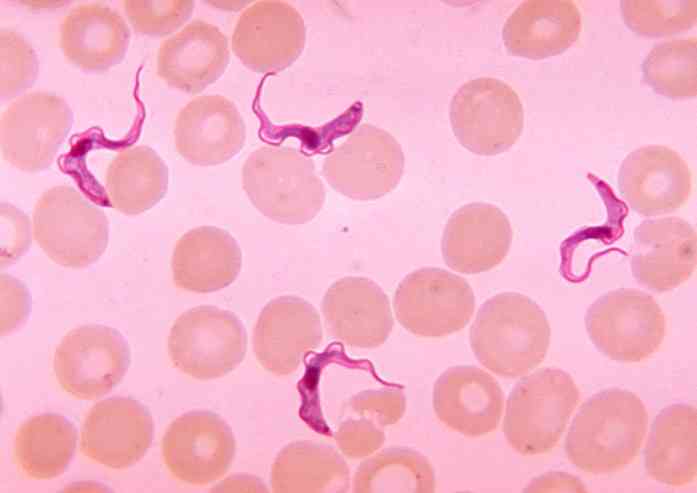
E betegség mindkét változatát jelentették a szubszaharai Afrika országaiban, ahol a tsetse-repülést találták, Glossina spp, a vektor vagy az átadó ágens T. brucei.
Egy harmadik alfaj, Trypanosoma brucei subsp. brucei, hasonló betegséget okoz a házi és a vadon élő állatokban, úgynevezett nagana.
Az alvó betegség több mint 60 millió embert fenyeget a szubszaharai Afrika 36 országában. Évente mintegy 300 000-500 000 eset van, ebből mintegy 70 000 és 100 000 között halnak meg. A tsetse-repülés fertőzése 10 millió négyzetkilométernyi területet ölel fel, Afrika földrészének egyharmadát.
Az Egészségügyi Világszervezet elismeri, hogy az utóbbi években jelentősen csökkent az afrikai humán trippanoszomiasis eseteinek száma. Ez annak köszönhető, hogy továbbra is fennállnak a nemzeti és nemzetközi kezdeményezések a betegség ellenőrzésére.
index
- 1 Általános jellemzők
- 1.1 A felfedezés
- 1.2 Genetika
- 1.3 Az "alvási betegség" és a globális felmelegedés
- 2 Phylogeny és taxonómia
- 3 Morfológia
- 3.1. Tryomastigote forma
- 3.2 Epimastigote forma
- 3.3 A kinetoszóma
- 4 Biológiai ciklus
- 4.1 A gazdaszervezetben (emberi vagy más emlős)
- 4.2 Tsetse fly (a vektor)
- 5 A fertőzés tünetei
- 5.1 Első fázis
- 5.2 Második fázis
- 5.3 Diagnózis
- 6 Kezelés
- 7 Referenciák
Általános jellemzők
"Alvási betegségnek" nevezik, mert a beteg természetes alvási ciklusának inverzióját okozza. A személy alszik a nap folyamán, és ébren marad éjjel. Ez a pszichés és neurológiai zavarok sorozatának eredménye, amelyet a betegség előrehaladott fázisában okoz.
A felfedezés
Az állati vagy nagana trippanosomiasis Afrikában a szarvasmarhák fontos betegsége. Ő azonosította magát Trypanosoma brucei David Bruce, miközben nagyméretű Zanuland-járvány kitörését vizsgálta..
Később Aldo Castellani azonosította ezt a trippanoszómafajtát az „alvó betegségben” szenvedő humán betegek vérében és cerebrospinális folyadékában..
1902 és 1910 között azonosították a betegség két variánsait és azok okozati alfajait. Mind az állatok, mind az emberek paraziták tárolóhelyei lehetnek, amelyek képesek az emberben a betegség okozására.
genetika
A gén genomja Trypanosoma brucei 11 diploid kromoszómából és száz mikrokromoszómából áll. Összesen 9.068 gént tartalmaz. A mitokondriumok genomja (a kinetoplaszt) a körkörös DNS számos példányából áll.
Az "alvó betegség" és a globális felmelegedés
Az afrikai humán trippanoszomiasist a 12 emberi fertőző betegség egyikének tekintik, amelyet a globális felmelegedés súlyosbíthat..
Ez annak a ténynek köszönhető, hogy amikor a környezeti hőmérséklet emelkedik, a repülés által elfoglalt terület nagyobb lesz. Glossina sp. A repülés új területeinek gyarmatosításakor magával ragadja a parazitát.
Phylogeny és taxonómia
Trypanosoma brucei pa Protista királysághoz tartozik, Excavata csoport, Euglenozoa, menedékjog, Kinetoplastidae osztály, Trypanosomatida, Trypanosomatidae család, nemzetség Trypanosoma, subgenre Tripanozoon.
Ennek a fajnak három alfaja van, amelyek különböző változatokat idéznek elő az „alvási betegség” emberekben (T. b. subsp. gambiense és T. b. subsp. rhodesiense), valamint a házi és a vadon élő állatok \ tT. b. subsp. brucei).
morfológia
Tripomastigote forma
Trypanosoma brucei egy 20 μm hosszú és 1-3 μm széles, hosszúkás, egysejtű szervezet, amelynek alakja, szerkezete és membránösszetétele az életciklusa alatt változik.
Két alapformája van. A mag és a hosszú gömböcske mögött álló bazális test tripomastigóta formája. Ez az űrlap viszont az életciklus alatt altípusokat feltételez. Ezek közül a rövid vagy makacs altípus (slumpy angolul), vastagabb és rövid ragyogása.
Epimastigote forma
A második alapforma az alaptest és a harangláb ellenkezője, az előzőtől kissé rövidebb..
A sejtet változó felületű glikoprotein réteg fedi. Ez a réteg megváltoztatja a felületének glikoproteinjeit, és így elfedi a gazdaszervezet által generált antitestek támadását.
Az immunrendszer új antitesteket termel a réteg új konfigurációjának megtámadására, és a réteg ismét megváltozik. Ez az úgynevezett antigén variáció.
A kinetosoma
Fontos jellemzője a kinetosoma jelenléte. Ez a szerkezet kondenzált mitokondriális DNS-ből áll, amelyek az egyetlen jelen lévő mitokondriumban találhatók. Ez a nagy mitokondrium a csapás alapja.
Biológiai ciklus
A. \ T Trypanosoma brucei váltakozik a tsetse között, mint egy vektor és az ember mint gazdaszervezet. Az ilyen különböző gazdaszervezetekben történő fejlődéshez a protozoon fontos metabolikus és morfológiai változásokat ér el egymástól.
A repülés közben a Trypanosoma brucei az emésztőrendszerben lakik, míg az emberben a vérben található.
A gazdaszervezetben (emberi vagy más emlős)
Trypanosoma brucei A ciklus során három alapformában van. Amikor a repülés emberi vagy más emlősöket harap ki a vér kivonására, a nyálmirigyéből a protozoonok nem-proliferatív formáját injektálja a véráramba..
Egyszer a véráramban a proliferatív formává alakul át, amelyet vékony vérnek neveznek.karcsú angolul).
A karcsú vérforma Trypanosoma brucei az energia a vérben lévő glükóz glikolíziséből származik. Ezt az anyagcsere-folyamatot egy glikozómának nevezett organellában végezzük. Ezek a trypanoszómák különböző testfolyadékokban szaporodnak: vér, nyirok és cerebrospinális folyadék.
Ahogy a paraziták száma a vérben növekszik, újra elkezd változni egy nem proliferatív formába. Ezúttal egy vastagabb variáns, rövidebb flagellummal, plump vérrel (tömzsi).
A csírázó vér trypanoszómák az emésztőrendszer körülményeihez igazodnak. Aktiválják mitokondriumaikat és a citromsav és a légzési lánc ciklusához szükséges enzimeket. Az energiaforrás már nem glükóz, hanem prolin.
A repülési tse-ben (a vektor)
A vektor vagy az adóvevő a Trypanosoma brucei ez a tse-tse repül, Glossina spp. Ez a nemzetség 25–30. Könnyen megkülönböztethetőek a közönséges repüléstől a különösen hosszú próbájukkal és a teljesen pihentetett szárnyaikkal.
Amikor egy tsetse-repülés harapja a fertőzött gazda emlősét és kivonja a vért, ezek a makacs vérformák behatolnak a vektorba.
Egyszer a légy emésztőrendszerében a makacs vérformák gyorsan differenciálódnak prociklikus proliferatív trippanoszomákká.
Bináris hasadással szaporodnak. Elhagyják a repülés emésztőrendszerét, és eljutnak a nyálmirigyekbe. Ezeket az epimastigotákká alakítják át, amelyeket a csapás a falakhoz rögzít.
A nyálmirigyekben szaporodnak és metaciklusos tripanoszomákká alakulnak, amelyek készen állnak az emlős vérrendszerébe történő beoltásra..
A fertőzés tünetei
Ennek a betegségnek az inkubációs periódusa 2-3 nappal a repülés harapása után. A T. b. Esetében néhány hónap után neurológiai tünetek jelentkezhetnek. subsp. gambiense. Ha erről van szó T. b. subsp. rhodesience, eltarthat évekig.
Első fázis
Az "alvó betegség" két szakaszból áll. Az elsőt korai stádiumnak vagy hemolimfás fázisnak nevezik, melyet a jelenléte jellemez Trypanosoma brucei csak a vérben és a nyirokban.
Ebben az esetben a tünetek láz, fejfájás, izomfájdalom, hányás, nyirokcsomók duzzanata, fogyás, gyengeség és ingerlékenység.
Ebben a fázisban a betegség összekeverhető a maláriával.
Második fázis
Az úgynevezett késői vagy neurológiai fázis (encephaliticus állapot) aktiválódik a parazita központi idegrendszerben való megérkezésével, melyet a cerebro-gerincfolyadékban detektálnak. Itt a tünetek a viselkedés, a zavartság, az összeegyeztethetetlenség, az alvási ciklus megváltoztatása és végül kóma.
A betegség kialakulása az alfajok esetében legfeljebb három éves ciklussal folytatódik gambiense, véget ért a halál. Amikor az alfaj jelen van rhodesience, a halál hetekről hónapokra.
A nem kezelt esetek 100% -a meghal. A kezelt esetek 2-8% -a is meghal.
diagnózis
A diagnosztikai stádium akkor van, amikor a fertőző forma, azaz a vér tripanoszomája megtalálható a vérben.
A vérminták mikroszkópos vizsgálatával kimutatható a parazita specifikus formája. Az encephalitikus fázisban a cerebrospinalis folyadék elemzéséhez lumbalis punkcióra van szükség.
Számos molekuláris technika létezik a jelenlét diagnosztizálására Trypanosoma brucei.
kezelés
A kapacitás Trypanosoma brucei a glikoproteinek külső rétegének (antigén variáció) állandó konfigurációjának megváltoztatása miatt nagyon nehéz a vakcinák kifejlesztése az "alvási betegség" ellen..
Nincs profilaktikus kemoterápia, és kevés vagy egyáltalán nem létezik vakcina. Az emberi afrikai trippanoszomiasisra használt négy fő gyógyszer toxikus.
A melarsoprol az egyetlen olyan gyógyszer, amely hatékony a központi idegrendszeri betegségek mindkét változatára. Ugyanakkor olyan mérgező, hogy a betegek 5% -át megöli.
Az eflornitint önmagában vagy nifurtimoxdal kombinálva egyre gyakrabban alkalmazzák a betegség által okozott betegség első soraként. Trypanosoma brucei subsp. gambiense.
referenciák
- K és K Matthews (2007) A Trypanosoma brucei differenciálódásának sejtbiológiája. Jelenlegi vélemény a mikrobiológiában. 10: 539-546.
- Fernández-Moya SM (2013) Az RBP33 és DRBD3 RNS-kötő fehérjék funkcionális jellemzése a gén expressziójának szabályozóiént Trypanosoma brucei. DOKTORI TÉZIS. "López-Neyra" parazitológiai és biomediciniai intézet. Granadai Szerkesztői Egyetem, Spanyolország. 189 p.
- García-Salcedo JA, D Pérez-Morga, P Gijón, V Dilbeck, E Pays és DP Nolan (2004) Az aktin differenciált szerepe a Trypanosoma brucei életciklusa alatt. Az EMBO Journal 23: 780-789.
- Kennedy PGE (2008) Az emberi afrikai trypanosomiasis (alvászavar) folyamatos problémája. Annals of Neurology, 64 (2), 116-126.
- Matthews KR (2005) Trypanosoma brucei. J. Cell Sci. 118, 283-290.
- Welburn SC, EM Fèvre, PG Coleman, M Odiit és I Maudlin (2001) Alvó betegség: két betegség története. TRENDEK a parazitológiában. 17 (1): 19-24.


