Ónklorid (SnCl2) Tulajdonságok, szerkezet, felhasználások és kockázatok
az ón-klorid (II) vagy ón-klorid, kémiai képlettel2, fehér kristályos szilárd anyag, az ón és a sósav koncentrált oldatának reakciója: Sn (s) + 2HCI (conc) => SnCl2(aq) + H2(G). A szintézisének (előkészítése) folyamata ónfólia darabok hozzáadásával áll a savval reagáltatni.
Az óndarabok hozzáadása után dehidratálást és kristályosodást hajtunk végre, amíg a szervetlen sót nem kapjuk. Ebben a vegyületben az ón elvesztette két elektronját a valens héjjából, hogy klóratomokkal kötéseket hozzon létre.
Ez jobban érthető, ha figyelembe vesszük az ón (5s) valencia konfigurációját25px2pés0pZ0), ebből az orbitálisan elfoglalt elektronok párjax a H protonoknak adjuk+, annak érdekében, hogy hidrogénből álló diatóma molekulát képezzen. Vagyis ez egy redox típusú reakció.
index
- 1 Fizikai és kémiai tulajdonságok
- 1.1 Valencia konfiguráció
- 1.2 Reakciókészség
- 1.3 Reduktív aktivitás
- 2 Kémiai szerkezet
- 3 Használat
- 4 Kockázatok
- 5 Referenciák
Fizikai és kémiai tulajdonságok
A SnCl linkek2 Ionos vagy kovalens? Az ón (II) -klorid fizikai tulajdonságai kizárják az első lehetőséget. A vegyület olvadási és forráspontja 247 ° C és 623 ° C, ami gyenge intermolekuláris kölcsönhatásokra utal, a kovalens vegyületek általános ténye.
Kristályai fehérek, amelyek a látható spektrumban nulla abszorpciót jelentenek.
Valencia konfigurációja
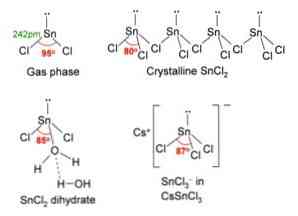
A fenti képen a bal felső sarokban egy izolált SnCl molekula látható2.
A molekuláris geometrianak síknak kell lennie, mivel a központi atom hibridizációja sp2 (3 orbitális sp2 és egy tiszta p orbitális, hogy kovalens kötéseket képezzen), de a szabad elektronpárok térfogatot foglalnak el, és a klóratomokat lefelé nyomják, így a molekulának szöggeometriája van.
A gázfázisban ezt a vegyületet izoláljuk, így nem lép kölcsönhatásba a többi molekulával.
Az orbitális elektronok elvesztése px, az ón átalakul az Sn ionba2+ és ennek az elektronikus konfigurációja 5 másodperc25px0pés0pZ0, az összes p orbitál elérhetővé teszi más fajok kapcsolatait.
Cl ionok- koordinálja a Sn iont2+ ón-kloridot kapunk. Az ón elektronikus konfigurációja ebben a sóban 5 másodperc25px2pés2pZ0, képes egy másik elektronpár elfogadására a szabad orbitális pZ.
Például elfogadhat egy másik Cl iont-, a trigonális sík geometriájának (háromszög alakú bázisú piramis) és negatív töltésű [SnCl3]-.
reakcióképesség
A SnCl2 nagy reaktivitással és hajlammal viselkedik, mint a Lewis-sav (elektron-receptor), hogy befejezze a valencia-oktettjét.
Ahogy elfogadja a Cl iont-, ugyanez történik a vízzel, amely "hidratálja" az ón atomot egy vízmolekula közvetlen összekapcsolásával az ónhoz, és egy második vízmolekula hidrogénkötő kölcsönhatásokat képez az első.
Ennek az az eredménye, hogy a SnCl2 nem tiszta, hanem a dihidrátos só: SnCl vízzel összehangolt2· 2H2O.
A SnCl2 Nagyon jól oldódik vízben és poláris oldószerekben, mert poláris vegyület. Vízben való oldhatósága azonban kisebb, mint a tömegtömege, ami hidrolízis reakciót (vízmolekula szakadását) aktiválja, hogy bázikus és oldhatatlan sót képezzen:
ón2(aq) + H2O (l) <=> Sn (OH) Cl (s) + HCI (aq)
A kettős nyíl azt jelzi, hogy egyensúly alakul ki, a bal oldali (a reaktánsok felé) előnyben részesítve, ha a HCl koncentráció nő. Ehhez a SnCl megoldások2 savak pH-ja van, hogy elkerüljük a hidrolízis nem kívánt sótermékének kicsapódását.
Reduktív aktivitás
Reagál oxigénnel a levegőben ón (IV) -klorid vagy ón-klorid előállítására:
6 SnCl2(aq) + O2(g) + 2H2O (l) => 2SnCl4(aq) + 4Sn (OH) Cl (s)
Ebben a reakcióban ón oxidálódik, amely kötést képez az elektronegatív oxigénatomhoz, és növeli a klóratomokkal való kötések számát.
Általában a halogének (F, Cl, Br és I) elektronegatív atomjai stabilizálják az Sn (IV) vegyületek kötését, és ez a tény magyarázza, hogy miért a SnCl2 redukálószer.
Amikor oxidálja és elveszíti az összes valenselektronját, az Sn ion4+ 5s-os konfigurációval marad05px0pés0pZ0, az 5-ös orbitális elektronok párja a legnehezebb, hogy „elkapják”.
Kémiai szerkezet
A SnCl2 egy orthombombikus típusú kristályszerkezetet mutat, hasonlóan a fűrészek soraihoz, amelyekben a fogak hegyei kloridok..
Minden sor SnCl lánc3 Cl híd képzése egy másik Sn atomdal (Cl-Sn (Cl)2-Cl- ···, ahogy a fenti képen látható. Két lánc, amelyet az Sn-Cl típus gyenge kölcsönhatásai kötnek össze, egy olyan réteget alkotnak, amely egy másik rétegre van ráhelyezve, és így tovább, amíg a kristályos szilárd anyagot meg nem határozzuk..
Az 5s szabad elektronpár2 torzulást okoz a struktúrában, mert térfogatot foglal el (az elektronikus felhő mennyisége).
Az Sn koordinátái száma megegyezhet a kilencével, ami ugyanaz, mint kilenc szomszédja, ezzel egy trigonális prizmát rajzolva ezzel a geometriai alak közepén, a Cl pedig a csúcsokban, a többi Cl mellett, mindegyikben a prizma szögletes arcai.
Ez könnyebben megfigyelhető, ha egy olyan láncot veszünk figyelembe, ahol az Sn (sötét szürke gömbök) felfelé mutatnak, és a három Cl kapcsolódik a háromszög alakú padlóhoz, míg a három felső Cl a háromszög alakú tetőt alkotja.
alkalmazások
A szerves szintézisben az aromás nitro-vegyületek redukálószerként (Ar-NO2 à Ar-NH2). Mivel a kémiai szerkezete lamináris, a világban a szerves reakciók katalízisét használja fel, amellett, hogy potenciálisan katalitikus hordozót jelent..
Redukáló tulajdonságát az arany vegyületek jelenlétének meghatározására, a szemüveg ezüst tükrökkel való bevonására és antioxidánsként való alkalmazására használják.
Emellett molekuláris geometriájában a trigonális piramis (SnX3- M+) Lewis bázisként használják nagyszámú vegyület (például a Pt klaszter komplex) szintéziséhez.3Sn8Cl20, ahol az elektronmentes pár Lewis-savval van összehangolva).
kockázatok
A SnCl2 Ez károsíthatja a fehérvérsejteket. Maró, irritáló, rákkeltő, és nagy negatív hatással van a tengeri ökoszisztémákat élő fajokra.
Magas hőmérsékleten bomlik, felszabadítva a káros klórgázt. Az erősen oxidáló szerekkel érintkezve robbanásveszélyes reakciókat vált ki.
referenciák
- Shiver & Atkins. (2008). Szervetlen kémia -ban A 14. csoport elemei (negyedik kiadás, 329. oldal). Mc Graw-hegy.
- ChemicalBook. (2017). 2018 március 21-én, a ChemicalBook-ból származik: chemicalbook.com
- Pubchem. (2018). Ónklorid. 2018 március 21-én, a PubChem-ből: pubchem.ncbi.nlm.nih.gov.
- Wikipedia. (2017). Ón (II) -klorid. Szerkesztve 2018. március 21-én, a Wikipédiából: en.wikipedia.org
- E. G. Rochow, E. W. (1975). A germánium kémia: ón és ólom (első szerk.). p-82,83. Pergamom Press.
- F. Hulliger. (1976). A réteg-fázisok szerkezeti kémia. P-120.121. D. Reidel Kiadó.



